Câu hỏi 1 :
Khi cho khí CO dư vào hỗn hợp CuO, FeO, Fe3O4, AlO3 và MgO. Nung nóng , sau khi các phản ứng xảy ra hoàn toàn thì thu được hỗn hợp là :
- A Cu, Fe, Al2O3, MgO
- B Al, MgO và Cu
- C Cu, Fe, Al và MgO
- D Cu, Al, Mg
Đáp án: A
Lời giải chi tiết:
Chỉ có oxit kim loại đứng sau Al mới bị các khử bởi các tác nhân trung bình (CO, C, H2…)
Đáp án A
Câu hỏi 2 :
Hai oxit nào sau đây bị khử bởi CO ở nhiệt độ cao?
- A ZnO và K2O.
- B Fe2O3 và MgO.
- C FeO và CuO.
- D Al2O3 và ZnO.
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 3 :
Để thu được kim loại Fe từ dung dịch Fe(NO3)2 theo phương pháp thuỷ luyện, có thể dùng kim loại nào sau đây:
- A Zn.
- B Fe.
- C Na.
- D Ca.
Đáp án: A
Lời giải chi tiết:
Đáp án A
Câu hỏi 4 :
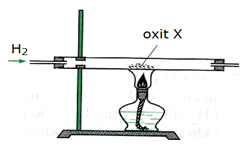
Để điều chế kim loại X người ta tiến hành khử oxit X bằng khí CO (dư) theo mô hình thí nghiệm dưới đây
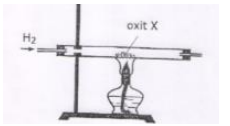
Oxit X là chất nào trong các chất sau
- A CaO
- B K2O
- C Al2O3
- D CuO
Đáp án: D
Lời giải chi tiết:
Dùng H2 để điều chế các kim loại bằng việc khử các oxit sau Al trong dãy điện hóa
Đáp án D
Câu hỏi 5 :
Dẫn luồng khí CO qua hỗn hợp Al2O3, CuO, MgO, Fe2O3 (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là
- A Al2O3,Cu,MgO,Fe .
- B Al2O3,Fe2O3,Cu,MgO
- C Al2O3,Cu,Mg,Fe .
- D Al,Fe,Cu,Mg.
Đáp án: A
Lời giải chi tiết:
Oxit của các kim loại sau Al mới bị khử bởi các tác nhân khử trung bình (CO, C, H2,…)
Đáp án A
Câu hỏi 6 :
Dẫn luồng khí CO dư qua hỗn hợp CuO, CaO, Al2O3, MgO có số mol bằng nhau (nung nóng ở nhiệt độ cao) thu được chất rắn A. Hòa tan A vào nước dư còn lại chất rắn X. X là:
- A Cu, Mg
- B Cu, Al2O3, MgO
- C Cu, MgO
- D Cu, Mg, Al2O3
Đáp án: C
Lời giải chi tiết:
CO chỉ khử được những oxit của kim loại đứng sau Al trong dãy điện hóa
+ Khi cho CO dư qua CuO, Al2O3, CaO, MgO có số mol bằng nhau (Giả sử số mol mỗi chất là 1 mol) ta thu được chất rắn A gồm: 1 mol Cu, 1 mol Al2O3, 1 mol CaO, 1 mol MgO
+ Hòa tan A vào nước dư:
CaO + H2O → Ca(OH)2
1 1
Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O
1 1
Vậy CaO và Al2O3 bị tan hết, chất rắn X gồm Cu, MgO
Đáp án C
Câu hỏi 7 :
Muốn điều chế Cu từ dung dịch CuSO4 theo phương pháp thủy luyện người ta dùng kim loại nào sau đây làm chất khử?
- A Na.
- B Ag.
- C Fe.
- D Ca.
Đáp án: C
Lời giải chi tiết:
Dùng Fe để điều chế Cu từ CuSO4 theo phương pháp thủy luyện
Fe + CuSO4 → FeSO4 + Cu↓
Đáp án C
Câu hỏi 8 :
Tiến hành phản ứng khử oxit X thành kim loại bằng khí H2 dư theo sơ đồ hình vẽ:
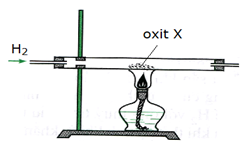
Oxit X không thể là:
- A CuO .
- B Al2O3.
- C PbO
- D FeO.
Đáp án: B
Lời giải chi tiết:
H2 chỉ khử được các oxit kim loại đứng sau Al trong dãy điện hóa
=> Không thể khử được oxit Al là Al2O3
Đáp án B
Câu hỏi 9 :
Có 4 muối : NaCl, CaCl2, Fe(NO3)2, Zn(NO3)2, AgNO3. Dùng phương pháp thủy luyện có thể điều chế được mấy kim loại từ dung dịch muối của nó?
- A 2
- B 3
- C 4
- D 5
Đáp án: B
Phương pháp giải:
*Phương pháp thủy luyện: Điều chế các kim loại đứng sau Al
- Kim loại mạnh đẩy kim loại yếu ra khỏi muối của nó
Lời giải chi tiết:
Phương pháp thủy luyện chỉ điều chế được các kim loại đứng sau Al =>
Có thể điều chế được Fe, Zn, Ag từ muối của nó
Đáp án B
Câu hỏi 10 :
Cho khí CO (dư) đi qua ống sứ đựng hỗn hợp X gồm: Al2O3, MgO, Fe3O4, CuO nung nóng thu được hỗn hợp rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm:
- A Một hợp chất và hai đơn chất.
- B Hai hợp chất và hai đơn chất.
- C Ba hợp chất và một đơn chất.
- D Ba đơn chất.
Đáp án: A
Phương pháp giải:
Chỉ có các oxit của kim loại đứng sau Al bị khử bởi CO.
Lời giải chi tiết:
Chỉ có các oxit của kim loại đứng sau Al bị khử bởi CO.
\(X\left\{ \begin{gathered}
A{l_2}{O_3} \hfill \\
MgO \hfill \\
F{e_3}{O_4} \hfill \\
CuO \hfill \\
\end{gathered} \right.\xrightarrow{{ + C{O_{du}}}}Y\left\{ \begin{gathered}
A{l_2}{O_3} \hfill \\
MgO \hfill \\
Fe \hfill \\
Cu \hfill \\
\end{gathered} \right.\xrightarrow{{ + NaO{H_{du}}}}Z\left\{ \begin{gathered}
MgO \hfill \\
Fe \hfill \\
Cu \hfill \\
\end{gathered} \right.\)
Đáp án A
Câu hỏi 11 :
Để tách Ag ra khỏi hỗn hợp Ag, Cu, Fe mà khối lượng Ag không thay đổi thì dùng chất nào sau đây?
- A HNO3.
- B Fe2(SO4)3.
- C AgNO3.
- D HCl.
Đáp án: B
Phương pháp giải:
Để tách Ag ra khỏi hỗn hợp Ag, Cu, Fe mà khối lượng Ag không thay đổi ta cần chọn chất phản ứng được với Cu và Fe mà không phản ứng với Ag.
Lời giải chi tiết:
Để tách Ag ra khỏi hỗn hợp Ag, Cu, Fe mà khối lượng Ag không thay đổi ta cần chọn chất phản ứng được với Cu và Fe mà không phản ứng với Ag. Chỉ có Fe2(SO4)3 thỏa mãn.
Đáp án B
Câu hỏi 12 :
Cho luồng khí H2 dư qua hỗn hợp các oxit CuO, Fe2O3, PbO, MgO nung ở nhiệt độ cao. Sau phản ứng hỗn hợp chất rắn gồm
- A Cu, Fe, Pb, MgO.
- B Cu, Fe, PbO, MgO.
- C Cu, Fe, Pb, Mg.
- D Cu, FeO, ZnO, MgO.
Đáp án: A
Phương pháp giải:
H2, CO, Al, C,… khử được những oxit của KL đứng sau Al trong dãy hoạt động hóa học.
Lời giải chi tiết:
- Oxit bị khử bởi H2 là: CuO, Fe2O3, PbO.
- Oxit không bị khử là: MgO
\(\left\{ \begin{array}{l}CuO + {H_2} \to Cu + {H_2}O\\F{{\rm{e}}_2}{O_3} + 3{H_2} \to 2F{\rm{e}} + 3{H_2}O\\PbO + {H_2} \to Pb + {H_2}O\\MgO\end{array} \right. \to \left\{ \begin{array}{l}Cu\\F{\rm{e}}\\Pb\\MgO\end{array} \right.\)
Đáp án A
Câu hỏi 13 :
Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3, MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm:
- A Cu, Al, Mg
- B Cu, Al, MgO
- C Cu, Al2O3, Mg
- D Cu, Al2O3, MgO
Đáp án: D
Phương pháp giải:
Khí CO có thể khử các oxit kim loại sau nhôm trong dãy hoạt động hóa học của kim loại.
Lời giải chi tiết:
Khí CO có thể khử các oxit kim loại sau nhôm trong dãy hoạt động hóa học của kim loại.
Vậy ở đây khí CO khử được CuO theo PTHH:
CO + CuO → Cu + CO2
Khi phản ứng hoàn toàn thu được chất rắn gồm Cu, Al2O3 và MgO.
Đáp án D
Câu hỏi 14 :
Dãy gồm 2 kim loại đều có thể điều chế bằng phương pháp thủy luyện là:
- A Fe và Ca
- B Mg và Na
- C Ag và Cu
- D Fe và Ba
Đáp án: C
Phương pháp giải:
Phương pháp thủy luyện dùng để điều chế các kim loại yếu như Ag và Cu.
Lời giải chi tiết:
Phương pháp thủy luyện dùng để điều chế các kim loại yếu như Ag và Cu.
Đáp án C
Câu hỏi 15 :
Sản phẩm thu được khi điện phân dung dịch KCl (điện cực trơ, màng ngăn xốp) là
- A K và Cl2.
- B K, H2 và Cl2.
- C KOH, H2 và Cl2.
- D KOH, O2 và HCl.
Đáp án: C
Phương pháp giải:
Phân tích sự điện phân ở mỗi điện cực. Từ đó viết được PT điện phân hoàn chỉnh.
Lời giải chi tiết:
Cl- (cực dương)← KCl, H2O → K+ (cực âm)
2Cl- → Cl2 + 2e 2H2O + 2e →H2+ 2OH-
PT điện phân:
2KCl + 2H2O → 2KOH + Cl2+ H2
Vậy sản phẩm thu được là KOH, Cl2, H2.
Đáp án C
Câu hỏi 16 :
Để thu được kim loại Cu từ dung dịch CuSO4 theo phương pháp thủy luyện, có thể dùng kim loại nào sau đây?
- A Ca.
- B Fe.
- C Na.
- D Ag.
Đáp án: B
Phương pháp giải:
Phương pháp thủy luyện là dùng kim loại mạnh hơn Cu đẩy Cu ra khỏi muối của nó (kim loại đứng từ Mg trở về sau trong dãy điện hóa học)
Lời giải chi tiết:
Dùng Fe đẩy muối CuSO4 ta thu được Cu
Fe + CuSO4 → FeSO4 + Cu↓
Đáp án B
Câu hỏi 17 :
Cho luồng khí H2 dư qua hỗn hợp oxit gồm : CO, Fe2O3 , ZnO, MgO nung ở nhiệt độ cao. Sau phản ứng thu được hỗn hợp rắn còn lại :
- A Fe, Zn, MgO.
- B Fe, ZnO, MgO
- C CO, Fe, ZnO, MgO.
- D CO, FeO, ZnO, MgO
Đáp án: A
Phương pháp giải:
Các chất khử trung bình : CO, C, H2 chỉ khử được các oxit sau Al trong dãy điện hóa học về kim loại
Lời giải chi tiết:
H2 và CO chỉ khử được Fe2O3 và ZnO
Fe2O3 + 3H2 → 2Fe + 3H2O
ZnO + H2 → Zn + H2O
Các chất rắn gồm : Fe, Zn, MgO
Đáp án A
Câu hỏi 18 :
Kim loại nào sau đây có thể điều chế bằng phản ứng thủy luyện?
- A Na.
- B Mg.
- C Cu.
- D Al.
Đáp án: C
Phương pháp giải:
Dựa vào kiến thức điều chế của kim loại
+ Nhóm kim loại IA, IIA, Al điều chế bằng phương pháp điện phân nóng chảy
+ Nhóm các kim loại trung bình, yếu điều chế được bằng phương pháp điện phân dung dịch, phương pháp thủy luyện
Lời giải chi tiết:
Na, Mg, Al điều chế bằng phương pháp điện phân nóng chảy
Cu có thể điều chế được bằng phương pháp thủy luyện
Đáp án C
Câu hỏi 19 :
Tiến hành các thí nghiệm sau
(a) Cho kim loại Cu vào dung dịch FeCl3 dư
(b) Điện phân dung dịch AgNO3 với điện cực trơ
(c) Nung nóng hỗn hợp bột Al và FeO ( không có không khí)
(d) Cho kim loại Ba vào dung dịch CuSO4 dư
(e) Điện phân Al2O3 nóng chảy
Số thí nghiệm tạo thành kim loại là
- A 4
- B 5
- C 3
- D 2
Đáp án: C
Phương pháp giải:
Viết PTHH xảy ra, chọn các phản ứng có tạo thành kim loại.
Lời giải chi tiết:
(a) không tạo thành kim loại do Cu + 2FeCl3 → 2FeCl2 + CuCl2
(b) Điện phân dung dịch AgNO3 với điện cực trơ tạo thành Ag
(c) 2Al + 3FeO → Al2O3 + 3Fe
(d) Cho kim loại Ba vào dung dịch CuSO4 dư không tạo kim loại do Ba tác dụng với nước tạo bazo
(e) Al2O3 đpnc tạo Al và O2
Đáp án C
Câu hỏi 20 :
Dãy gồm các kim loại đều có thể điều chế được bằng phương pháp nhiệt luyện là
- A Fe, Cu, Pb.
- B Fe, Cu, Ba.
- C Na, Fe, Cu.
- D Ca, Al, Fe.
Đáp án: A
Phương pháp giải:
Phương pháp nhiệt luyện (dùng kim loại mạnh để đẩy kim loại yếu ra khỏi dung dịch muối) => dùng để điều chế các kim loại từ Mg trở về sau trong dãy điện hóa
Lời giải chi tiết:
Phương pháp nhiệt luyện (dùng kim loại mạnh để đẩy kim loại yếu ra khỏi dung dịch muối) => dùng để điều chế các kim loại từ Mg trở về sau trong dãy điện hóa
A. thỏa mãn
B. loại Ba
C. Loại Na.
D. Loại Ca
Đáp án A
Câu hỏi 21 :
Kim loại nào sau đây được điều chế bằng phản ứng nhiệt luyện?
- A Ca.
- B Fe.
- C Al.
- D Na.
Đáp án: B
Phương pháp giải:
Phương pháp nhiệt luyện:dùng các chất khử như C, H2, CO, Alđể khử các oxi kim loại có tính khử trung bình để điều chế kim loại. (Các kim loại đứng sau Al)
Lời giải chi tiết:
Fe có thể được điều chế bằng phương pháp nhiệt luyện
VD: H2+ FeO \(\buildrel {{t^0}} \over\longrightarrow \) Fe + H2O
Đáp án B
Câu hỏi 22 :
Ở nhiệt độ cao, khí H2 khử được oxit nào sau đây?
- A Al2O3.
- B MgO.
- C CuO.
- D CaO.
Đáp án: C
Phương pháp giải:
Chất khử trung bình (C, CO, H2) chỉ khử được những oxit của những kim loại đứng sau Al trong dãy điện hóa.
Lời giải chi tiết:
Chất khử trung bình (C, CO, H2) chỉ khử được những oxit của những kim loại đứng sau Al trong dãy điện hóa.
Do đó H2 chỉ có thể khử được oxit CuO
Đáp án C
Câu hỏi 23 :
Dẫn khí CO dư qua hỗn hợp bột Al2O3, Fe2O3 đun nóng đến khi phản ứng hoàn toàn thu được hỗn hợp rắn gồm:
- A Al, Fe
- B Al, FeO
- C Al2O3, Fe
- D Al2O3, FeO
Đáp án: C
Phương pháp giải:
Chất khử trung bình (C, CO, H2) chỉ khử được những oxit của những kim loại đứng sau Al trong dãy điện hóa.
Lời giải chi tiết:
Chất khử trung bình (C, CO, H2) chỉ khử được những oxit của những kim loại đứng sau Al trong dãy điện hóa.
Do đó CO chỉ có thể khử được oxit Fe2O3 thành Fe
=> Hỗn hợp rắn gồm: Al2O3, Fe
Đáp án C
Câu hỏi 24 :
Hình vẽ sau đây mô tả thí nghiệm khi cho khí X tác dụng với chất rắn Y, nung nóng sinh rakhí Z:
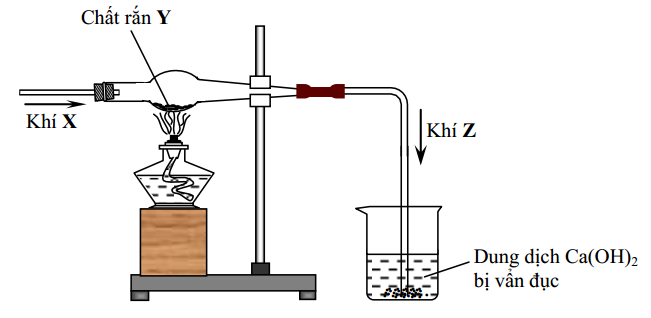
Phương trình hóa học tạo thành khí Z là
- A \(CuO + CO\xrightarrow{{{t^0}}}Cu + C{O_2}\)
- B CaCO3 + 2HCl → CaCl2 + CO2 + H2O
- C \(F{e_2}{O_3} + 3{H_2}\xrightarrow{{{t^0}}}2Fe + 3{H_2}O\)
- D \(CuO + {H_2}\xrightarrow{{{t^0}}}Cu + {H_2}O\)
Đáp án: A
Phương pháp giải:
Dựa vào kĩ năng quan sát sơ đồ thí nghiệm
Lời giải chi tiết:
Từ hình vẽ ta dễ dàng nhận ra được khí Z là khí CO2 . Từ đó loại được đáp án C và D
khí Z được sinh ra bằng cách cho khí X tác dụng với rắn Y
=> khí X là CO; rắn Y là CuO
Vậy phương trình hóa học tạo thành khí CO2 thỏa mãn là
\(CuO + CO\xrightarrow{{{t^0}}}Cu + C{O_2}\)
Đáp án A
Câu hỏi 25 :
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư;
(b) Sục khí Cl2 vào dung dịch FeCl2;
(c) Dẫn khí H2 dư qua bột CuO nung nóng;
(d) Cho Na vào dung dịch MgSO4 dư;
(e) Nhiệt phân Cu(NO3)2;
(g) Đốt FeS2 trong không khí;
(h) Điện phân dung dịch AgNO3 với điện cực trơ;
(i) Cho AgNO3 vào dung dịch Fe(NO3)2 dư;
(k) Sục khí CO2 dư vào dung dịch muối natri aluminat.
Sau khi kết thúc phản ứng, số thí nghiệm thu được kim loại là
- A 4
- B 3
- C 2
- D 5
Đáp án: B
Phương pháp giải:
Viết PTHH từ đó xác định những thí nghiệm sinh ra kim loại sau phản ứng.
Lời giải chi tiết:
(a) 3Mg + 3Fe2(SO4)3 dư → 3MgSO4 + 6FeSO4 => không thu được kim loại
(b) Cl2 + FeCl2 → FeCl3 => không thu được kim loại
(c) H2 + CuO \(\xrightarrow{{{t}^{o}}}\) Cu + H2O => thu được kim loại Cu
(d) 2Na + 2H2O → 2NaOH + H2; 2NaOH + MgSO4 dư → Mg(OH)2 + Na2SO4 => không thu được kim loại
(e) 2Cu(NO3)2 \(\xrightarrow{{{t}^{o}}}\) 2CuO + 4NO2 + O2 => không thu được kim loại
(g) 4FeS2 + 11O2 \(\xrightarrow{{{t}^{o}}}\) 2Fe2O3 + 8SO2 => không thu được kim loại
(h) 4AgNO3 + 2H2O \(\xrightarrow{dp\text{dd}}\) 4Ag + 4HNO3 + O2 => thu được kim loại Ag
(i) AgNO3 + Fe(NO3)2 dư → Fe(NO3)3 + Ag => thu được kim loại Ag
(k) CO2 dư + NaAlO2 + 2H2O → Al(OH)3 + NaHCO3 => không thu được kim loại
Vậy có 3 thí nghiệm thu được kim loại sau phản ứng.
Đáp án B
Câu hỏi 26 :
Tiến hành các thí nghiệm sau:
(a) Cho kim loại Na vào dung dịch CuSO4
(b) Dẫn khí CO dư qua Al2O3 nung nóng
(c) Cho kim loại Mg vào dung dịch CuSO4
(d) Điện phân dung dịch CaCl2 có màng ngăn
Số thí nghiệm thu được kim loại là
- A 1
- B 2
- C 3
- D 4
Đáp án: A
Phương pháp giải:
Viết PTHH xảy ra
Lời giải chi tiết:
(a) Na + H2O → NaOH + H2↑
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
(b) CO không có pư vói Al2O3 nung nóng
(c) Mg + CuSO4 → MgSO4 + Cu↓
(d) CaCl2 + H2O \(\xrightarrow{{DPMN}}\) Ca(OH)2 + H2↑ + Cl2↑
chỉ có 1 thí nghiệm (c) thu được kim loại
Đáp án A
Câu hỏi 27 :
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl với điện cực trơ, thu được khí H2 ở catot
(b) Dùng khí CO dư khử CuO nung nóng, thu được kim loại Cu
(c) Để hợp kim Fe- Ni ngoài không khí ẩm thì kim loại Ni bị ăn mòn điện hóa học
(d) Dùng dung dịch Fe2(SO4)3 dư có thể tách Ag ra khỏi hỗn hợp Ag và Cu
(e) Cho Fe dư vào dung dịch AgNO3 sau phản ứng thu được dung dịch chứa hai muối
Số phát biểu đúng là
- A 2
- B 5
- C 3
- D 4
Đáp án: C
Phương pháp giải:
Xem lại lý thuyết tổng hợp hóa 12
Lời giải chi tiết:
(a) Đúng vì tại catot (-) có 2H2O + 2e → 2OH- + H2
(b) Đúng
(c) Sai vì Fe mạnh hơn Ni trong dãy điện hóa nên xảy ra ăn mòn Fe
(d) Đúng vì Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → tách Ag ra khỏi hỗn hợp Ag và Cu
(e) Sai vì chỉ tạo muối Fe(NO3)2
Đáp án C
Câu hỏi 28 :
Tiến hành các thí nghiệm sau:
(1) Cho Mg vào dung dịch Fe2(SO4)3 dư
(2) Sục khí Cl2 vào dung dịch CuSO4 dư
(3) Dẫn khí CO dư qua bột CuO nung nóng
(4) Cho Ba vào dung dịch CuSO4 dư
(5) Nung hỗn hợp Cu(OH)2 và (NH4)2CO3 trong bình kín
(6) Đốt FeS2 trong không khí
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
- A 1
- B 3
- C 4
- D 2
Đáp án: D
Phương pháp giải:
Viết PTHH của các phản ứng từ đó xác định được thí nghiệm sinh ra kim loại sau phản ứng.
Lời giải chi tiết:
(1) Mg + Fe2(SO4)3 dư → MgSO4 + 2FeSO4
=> Không thu được kim loại
(2) Cl2 + H2O \( \rightleftarrows \) HCl + HClO
=> Không thu được kim loại
(3) CO + CuO \(\xrightarrow{{{t^o}}}\) Cu + H2O
=> Thu được kim loại Cu
(4) Ba + 2H2O → Ba(OH)2 + H2
Ba(OH)2 + CuSO4 → Cu(OH)2 + BaSO4
=> Không thu được kim loại
(5) (NH4)2CO3 \(\xrightarrow{{{t^o}}}\) 2NH3 + H2O + CO2
Cu(OH)2 \(\xrightarrow{{{t^o}}}\) CuO + H2O
3CuO + 2NH3 \(\xrightarrow{{{t^o}}}\) 3Cu + N2 + 3H2O
=> Thu được kim loại Cu
(6) 4FeS2 + 11O2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 8SO2
=> Không thu được kim loại
Vậy có 2 thí nghiệm thu được kim loại
Đáp án D
Câu hỏi 29 :
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (điện cực trơ, có màng ngăn), thu được khí Cl2 ở catot.
(b) Cho CO dư qua hỗn hợp Fe2O3 và CuO đun nóng, thu được Fe và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại dẻo nhất là Au, kim loại có nhiệt độ nóng chảy thấp nhất là Hg.
(e) Để điều chế kim loại nhôm người ta điện phân nóng chảy Al2O3. Số phát biểu đúng là
- A 3
- B 4
- C 5
- D 2
Đáp án: B
Phương pháp giải:
Xem lại lý thuyết tổng hợp
Lời giải chi tiết:
(a) sai vì khí Cl2 ở anot.
(b) đúng
(c) đúng vì ban đầu Zn + CuSO4 → ZnSO4 +Cu → xuất hiện hai kim loại Cu, Zn tiếp xúc với nhau và cùng tiếp xúc với môi trường điện ly→ có xuất hiện ăn mòn điện hóa.
(d) đúng
(e) đúng
→ Số phát biểu đúng là 4
Đáp án B
Câu hỏi 30 :
Tiến hành các thí nghiệm:
(a) Cho AgNO3 vào dung dịch Fe(NO3)2.
(b) Dẫn NH3 qua ống đựng CuO nung nóng.
(c) Nhiệt phân AgNO3.
(d) Cho Al vào dung dịch Fe2(SO4)3 dư.
(e) Cho K vào dung dịch Cu(NO3)2.
Sau khi kết thúc các phản ứng, số thí nghiệm có tạo thành kim loại là
- A 2
- B 1
- C 3
- D 4
Đáp án: C
Phương pháp giải:
Viết PTHH
Lời giải chi tiết:
(a) AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag → tạo kim loại Ag
(b) 2NH3 + 3CuO → 3Cu↓+ N2↑ + 3H2O → tạo kim loại Cu
(c) 2AgNO3 \(\xrightarrow{{{t^o}}}\) 2Ag↓ + 2NO2 + O2↑→ tạo kim loại Ag
(d) 2Al + Fe2(SO4)3 dư → 2FeSO4 + Al2(SO4)3 → không tạo kim loại
(e) K + H2O → KOH + ½ H2 rồi Cu(NO3)2 + 2KOH → 2KNO3 + Cu(OH)2↓ → không tạo kim loại
→ có 3 thí nghiệm tạo kim loại
Đáp án C
Câu hỏi 31 :
Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3, MgO, nung nóng ở nhiệt độ cao. Sau khi phản ứng xảy ra hoàn toàn, hỗn hợp chất rắn thu được là
- A Cu, Al2O3, Mg.
- B Cu, Al, Mg.
- C Cu, Al, MgO.
- D
Cu, Al2O3, MgO.
Đáp án: D
Phương pháp giải:
CO chỉ khử được các oxi kim loại đứng sau Al trong dãy điện hóa
Lời giải chi tiết:
CO chỉ khử được các oxi kim loại đứng sau Al trong dãy điện hóa
\(CO\,du + \left\{ \matrix{
CuO \hfill \cr
A{l_2}{O_3} \hfill \cr
MgO \hfill \cr} \right.\buildrel {{t^0}} \over
\longrightarrow \left\{ \matrix{
Cu \hfill \cr
A{l_2}{O_3} \hfill \cr
MgO \hfill \cr} \right.\)
Đáp án D
Câu hỏi 32 :
Kim loại nào sau đây điều chế được bằng phương pháp nhiệt luyện với chất khử là H2?
- A K.
- B Na.
- C Fe.
- D Ca.
Đáp án: C
Phương pháp giải:
Dựa vào kiến thức trong bài điều chế kim loại - sgk hóa 12
Các kim loại đứng sau Mg trong dãy điện hóa có thể được điều chế bằng phương pháp nhiệt luyện
Lời giải chi tiết:
Fe được điều chế bằng phương pháp nhiệt luyện
Đáp án C
Câu hỏi 33 :
Cho luồng khí H2 (dư) qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung ở nhiệt độ cao. Sau khi phản ứng xảy ra hoàn toàn, hỗn hợp rắn còn lại:
- A Cu, Fe, Zn, Mg
- B Cu, Fe, Zn, MgO
- C Cu, FeO, ZnO, MgO
- D Cu, Fe, ZnO, MgO
Đáp án: B
Phương pháp giải:
Các chất có tính khử trung bình (C, CO, H2, Al) chỉ có thể khử oxit của kim loại đứng sau Al trong dãy điện hóa học.
Lời giải chi tiết:
Các chất có tính khử trung bình (C, CO, H2, Al) chỉ có thể khử oxit của kim loại đứng sau Al trong dãy điện hóa học.
Như vậy H2 không phản ứng được với MgO
=> Chất rắn còn lại chứa: Cu, Fe, Zn, MgO
Đáp án B
Câu hỏi 34 :
Cho luồng khí H2 dư qua hỗn hợp các oxit sau : CuO, Fe2O3, ZnO, MgO nung ở nhiệt độ cao. Sau phản ứng hoàn toàn hỗn hợp rắn còn lại là
- A
Cu, Fe, Zn, MgO.
- B
Cu, Fe, ZnO, MgO.
- C
Cu, Fe, Zn, Mg.
- D
Cu, FeO, ZnO, MgO.
Đáp án: A
Phương pháp giải:
Lý thuyết về phương pháp nhiệt luyện trong điều chế kim loại.
Lời giải chi tiết:
Hiđro khử được các oxit sau nhôm → hỗn hợp rắn sau phản ứng là Cu, Fe, Zn, MgO
Đáp án A
Câu hỏi 35 :
Từ mỗi chất Cu(OH)2, NaCl, FeS2, lựa chọn phương pháp thích hợp (các điều kiện khác có đủ) để điều chế ra các kim loại tương ứng. Khi đó, số phản ứng hoá học tối thiểu phải thực hiện để điều chế được 3 kim loại Cu, Na, Fe là
- A
3.
- B 4.
- C 5.
- D 6.
Đáp án: C
Lời giải chi tiết:
\(Cu(OH)_2 \xrightarrow{{t^0}} CuO + H_2O\)
\( CuO+H_2 \to Cu +H_2\)
\(NaCl \xrightarrow{{đpnc}} Na + 1/2 Cl_2\)
\(4FeS_2 +11O_2 \to 2Fe_2O_3 + 8SO_2\)
\(Fe_2O_3 +3CO\to 2Fe + 3CO_2\)
Đáp án C
Câu hỏi 36 :
Từ các chất riêng biệt: CuSO4, CaCO3, FeS để điều chế được các kim loại Cu, Ca, Fe thì số phản ứng hoá học tối thiểu phải thực hiện là (các điều kiện khác có đủ)
- A
4.
- B 5.
- C 6.
- D 7.
Đáp án: B
Lời giải chi tiết:
\(CuSO_4 + H_2O\xrightarrow{{đpdd}} Cu + H_2SO_4 + 1/2O_2\)
\(CaCO_3 +HCl \to CaCl_2 +CO_2 + H_2O\)
\(CaCl_2 \xrightarrow{{đ pnc}} Ca + Cl_2\)
\(FeS+ 2HCl \to FeCl_2 + H_2O\)
\(FeCl_2 \xrightarrow {{đpdd}} Fe+ Cl_2\)
Đáp án B
Câu hỏi 37 :
Trong quá trình điện phân dung dịch CuSO4 với các điện cực bằng Cu, nhận thấy:
- A nồng độ ion Cu2+ trong dung dịch tăng dần.
- B nồng độ ion Cu2+ trong dung dịch giảm dần.
- C nồng độ Cu2+ trong dung dịch không thay đổi.
- D chỉ có nồng độ ion SO42- là thay đổi.
Đáp án: C
Phương pháp giải:
Lý thuyết về phản ứng điện phân.
Lời giải chi tiết:
Bán phản ứng tại các điện cực:
Catot (-): Cu2+ + 2e → Cu
Anot (+): Cu → Cu2+ + 2e
Trong quá trình điện phân dung dịch CuSO4 với các điện cực bằng Cu, nhận thấy nồng độ ion Cu2+ trong dung dịch không đổi do ở cực âm quá trình khử ion đồng, cực dương quá trình oxi hóa đồng.
Đáp án C
Câu hỏi 38 :
Cho các cách điều chế kim loại Cu từ Cu(NO3)2 và Ca từ CaCl2 như sau:
(1) 2Cu(NO3)2 + 2H2O \(\xrightarrow{{dpdd}}\) 2Cu + 4HNO3 + O2
(2) Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
(3) 2Na + Cu(NO3)2 → 2NaNO3 + Cu
(4) 2Cu(NO3)2 \(\xrightarrow{{{t^o}}}\) 2CuO + 4NO2 + O2
CuO + CO \(\xrightarrow{{{t^o}}}\) Cu + CO2
(5) CaCl2 \(\xrightarrow{{dpnc}}\) Ca + Cl2
(6) CaCl2 + Ba → BaCl2 + Ca
Số cách điều chế đúng là
- A 3.
- B 4.
- C 5.
- D 6.
Đáp án: B
Phương pháp giải:
Lý thuyết về điều chế kim loại.
Lời giải chi tiết:
- Điều chế Cu từ Cu(NO3)2:
(1) 2Cu(NO3)2 + 2H2O \(\xrightarrow{{dpdd}}\) 2Cu + 4HNO3 + O2
(2) Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
(4) 2Cu(NO3)2 \(\xrightarrow{{{t^o}}}\) 2CuO + 4NO2 + O2
CuO + CO \(\xrightarrow{{{t^o}}}\) Cu + CO2
- Điều chế Ca từ CaCl2:
(5) CaCl2 \(\xrightarrow{{dpnc}}\) Ca + Cl2
Vậy có 4 cách điều chế đúng.
Đáp án B
Câu hỏi 39 :
Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3 và MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm
- A
Cu, Al, Mg.
- B
Cu, Al, MgO.
- C
Cu, Al2O3, Mg.
- D
Cu, Al2O3, MgO.
Đáp án: D
Phương pháp giải:
Ở nhiệt độ cao, khí CO khử được các oxit của kim loại sau nhôm trong dãy điện hóa.
Lời giải chi tiết:
Ở nhiệt độ cao, khí CO khử được các oxit của kim loại sau nhôm trong dãy điện hóa.
Vậy nên cho CO qua hỗn hợp CuO, Al2O3, MgO (nung nóng) thì CO chỉ khử được CuO, không khử được Al2O3 và MgO.
PTHH: \(CO + CuO\xrightarrow{{{t^o}}}Cu + C{O_2}\)
Vậy chất rắn thu được sau phản ứng chứa: Cu, Al2O3 và MgO.
Đáp án D
Câu hỏi 40 :
Trình bày phương pháp hoá học để có thể tách riêng từng kim loại ra khỏi một dung dịch có chứa các muối:
a) FeSO4 và CuSO4.
b) NaCl và CuCl2.
Phương pháp giải:
a) Cho sắt vào dung dịch thu được Cu sau đó thu được dung dịch FeSO4 → đưa về \(Fe_2O_3\) → dùng CO khử
b) Dùng NaOH → thu được dd NaCl điện phân nóng chảy thu được Na. Nung kết tủa \(Cu(OH)_2\) → CuO dùng CO khử
Lời giải chi tiết:
a)
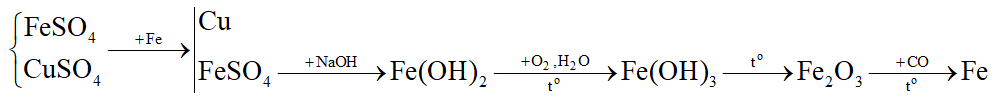
Các PTHH:
\(F{\rm{e}} + CuS{O_4} \to F{\rm{eS}}{{\rm{O}}_4} + Cu\)
\(F{\rm{eS}}{{\rm{O}}_4} + 2NaOH \to F{\rm{e}}{(OH)_2} + N{a_2}S{O_4}\)
\(4F{\rm{e}}{(OH)_2} + {O_2} + 2{H_2}O \to 4F{\rm{e}}{(OH)_3}\)
\(2F{\text{e}}{(OH)_3}\xrightarrow{{{t^o}}}F{{\text{e}}_2}{O_3} + 3{H_2}O\)
\(F{{\text{e}}_2}{O_3} + 3CO\xrightarrow{{{t^o}}}F{\text{e}} + 3C{O_2}\)
b)
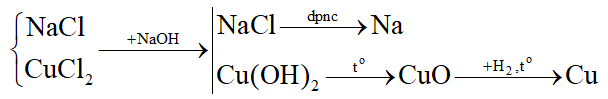
Các PTHH:
\(CuC{l_2} + 2NaOH \to Cu{(OH)_2} + 2NaCl\)
\(2NaCl\xrightarrow{{dpnc}}2Na + C{l_2}\)
\(Cu{(OH)_2}\xrightarrow{{{t^o}}}CuO + {H_2}O\)
\(CuO + {H_2}\xrightarrow{{{t^o}}}Cu + {H_2}O\)
Câu hỏi 41 :
Trình bày sơ đồ tách riêng từng kim loại từ hỗn hợp các kim loại: Cu, Fe, Al, Ag.
Phương pháp giải:
- Dùng \(H_2SO_4\) tách Fe, Al, và Cu, Ag thu được dung dịch X
- Dùng \(AgNO_3\) để tách Ag → Thêm Cu vào dung dịch thu được để thu được \(Cu(NO_3)_2\) sau đó điện phân dung dịch
- Dùng NaOH dư vào dung dịch X thu được chất rắn \(Fe(OH)_2\) và dung dịch Y
- \(Fe(OH)_2\) \(\to \) \(Fe_2O_3\) dùng CO khử
- Thêm \(CO_2\) vào dung dịch Y thu được \(Al(OH)_3\) -> \(Al_2O_3\) sau đó điện phân nóng chảy thu được Al
Lời giải chi tiết:
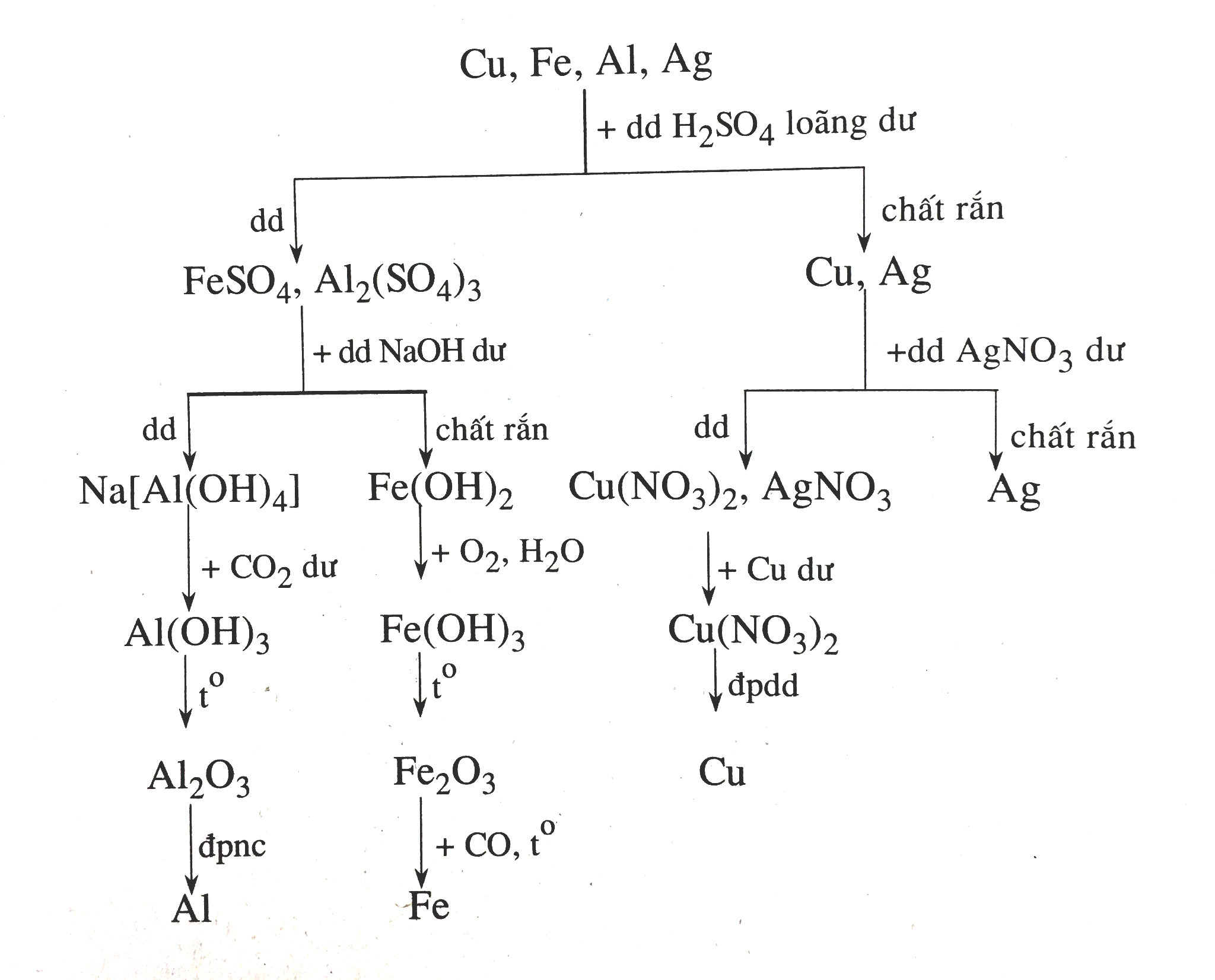
Câu hỏi 42 :
Kim loại nào sau đây có thể điều chế được bằng phương pháp thủy luyện?
- A Ba.
- B K.
- C Na.
- D Cu.
Đáp án: D
Phương pháp giải:
Phương pháp thủy luyện:
- Nguyên tắc: Dùng dung dịch thích hợp (HCl, HNO3, nước cường toan, CN-…) hòa tan nguyên liệu sau đó lấy kim loại mạnh (không tan trong nước) đẩy kim loại yếu khỏi dung dịch của nó.
- Phạm vi sử dụng: Thường dùng trong phòng thí nghiệm để điều chế các kim loại sau Mg (thường là kim loại yếu).
Lời giải chi tiết:
- Kim loại Cu có thể điều chế được bằng phương pháp thủy luyện.
- Các kim loại K, Na, Ba chỉ có thể điều chế bằng phương pháp điện phân nóng chảy hợp chất của chúng.
Đáp án D
Câu hỏi 43 :
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
- A Mg.
- B Fe.
- C Na.
- D Al.
Đáp án: B
Phương pháp giải:
Phương pháp nhiệt luyện là phương pháp dùng các chất khử như CO, H2, Al để khử các oxit của kim loại thành kim loại tương ứng.
Phương pháp này dùng để điều chế các kim loại từ Zn trở về sau trong dãy điện hóa học của kim loại.
Lời giải chi tiết:
Phương pháp nhiệt luyện dùng để điều chế các kim loại có tính khử trung bình yếu → Fe được điều chế bằng phương pháp này.
Đáp án B
Câu hỏi 44 :
Dẫn khí CO dư đi qua hỗn hợp X gồm MgO, CuO và Fe2O3, nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn Y gồm
- A MgO, Fe2O3, Cu.
- B Mg, Fe và Cu.
- C MgO, Fe và Cu.
- D MgO, Fe3O4, Cu.
Đáp án: C
Phương pháp giải:
CO chỉ khử được các oxit của KL đứng sau Al trong dãy điện hóa tạo thành kim loại.
Lời giải chi tiết:
CO chỉ khử được các oxit của KL đứng sau Al trong dãy điện hóa tạo thành kim loại
⟹ CO khử được CuO và Fe2O3
\(CO + CuO\xrightarrow{{{t^o}}}Cu + C{O_2}\)
\(3CO + F{{\text{e}}_2}{O_3}\xrightarrow{{{t^o}}}F{\text{e}} + 3C{O_2}\)
⟹ Chất rắn Y chứa: MgO, Cu và Fe
Đáp án C
Câu hỏi 45 :
Cho luồng khí H2 (dư) qua hỗn hợp các oxit CuO, Fe2O3, MgO nung nóng ở niệt độ cao. Sau khi phản ứng xảy ra hoàn tàn, hỗn hợp rắn còn lại là
- A Cu, FeO, MgO.
- B Cu, Fe, Mg.
- C CuO, Fe, MgO.
- D Cu, Fe, MgO.
Đáp án: D
Phương pháp giải:
H2 chỉ khử được các oxit của kim loại sau Al trong dãy hoạt động hóa học
Lời giải chi tiết:
PTHH: H2 + CuO \(\xrightarrow{{{t^0}}}\) Cu + H2O
H2 + Fe2O3 \(\xrightarrow{{{t^0}}}\)Fe + 3H2O
MgO không có pư với H2
Sau khi phản ứng xảy ra hoàn toàn hỗn hợp rắn thu được gồm: Cu, Fe và MgO
Đáp án D
Câu hỏi 46 :
Kim loại nào sau đây không được điều chế bằng phương pháp thủy luyện
- A Mg.
- B Fe.
- C Cu.
- D Ag.
Đáp án: A
Lời giải chi tiết:
Đáp án A
Câu hỏi 47 :
Kim loại nào sau đây hiện nay được điều chế chủ yếu bằng phương pháp nhiệt luyện?
- A Al.
- B Ca.
- C Fe.
- D Na.
Đáp án: C
Phương pháp giải:
Phương pháp nhiệt luyện là dùng các chất khử như C, CO, H2, Al để khử các oxit của kim loại có tính khử trung bình và yếu (từ Al trở về sau trong dãy điện hóa học của kim loại)

Lời giải chi tiết:
Phương pháp nhiệt luyện là dùng các chất khử như C, CO, H2, Al để khử các oxit của kim loại có tính khử trung bình và yếu.
Fe là kim loại có tính khử trung bình nên chủ yếu được điều chế bằng phương pháp nhiệt luyện.
Đáp án C
Câu hỏi 48 :
Từ dung dịch Cu(NO3)2 có thể điều chế Cu bằng cách:
- A cô cạn dung dịch rồi nhiệt phân muối rắn Cu(NO3)2.
- B cô cạn dung dịch rồi điện phân nóng chảy Cu(NO3)2.
- C dùng Fe khử Cu2+ trong dung dịch Cu(NO3)2.
- D Tất cả đều đúng.
Đáp án: C
Phương pháp giải:
1. Phương pháp nhiệt luyện: Điều chế các kim loại đứng sau Al
Oxit kim loại + CO, H2, Al, C Kim loại
2. Phương pháp thủy luyện: Điều chế các kim loại đứng sau Al
- Kim loại mạnh đẩy kim loại yếu ra khỏi muối của nó
3. Điện phân dung dịch:
- Điện phân nóng chảy:Điều chế kim loại trước Al
- Điện phân dung dịch: Điều chế kim loại sau Al
Lời giải chi tiết:
=> để điều chế Cu từ muối Cu(NO3)2 ta dùng Fe đẩy Cu ra khỏi muối
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Đáp án C
Câu hỏi 49 :
Dẫn khí CO dư đi qua hỗn hợp X gồm MgO, CuO và Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn Y gồm
- A Mg, Fe và Cu.
- B MgO, Fe và Cu.
- C MgO, Fe3O4, Cu.
- D MgO, Fe2O3, Cu.
Đáp án: B
Phương pháp giải:
CO và H2 khử được các oxit của kim loại đứng sau Al trong dãy hoạt động hóa học
Lời giải chi tiết:
CuO và Fe2O3 bị khử, MgO không bị khử bởi CO.
Chất rắn sau phản ứng là MgO, Cu, Fe.
Đáp án B
Câu hỏi 50 :
Tiến hành phản ứng khử oxi X thành kim loại bằng khí CO (dư) theo sơ đồ hình vẽ:
Oxit X là
- A Al2O3.
- B FeO.
- C K2O.
- D MgO.
Đáp án: B
Phương pháp giải:
Những oxit của kim loại đứng sau Al trong dãy hoạt động hóa học của KL bị khử bởi C, CO, H2.
Lời giải chi tiết:
Trong các đáp án chỉ FeO bị khử bởi H2 để tạo thành kim loại.
Đáp án B