Câu hỏi 1 :
Đốt cháy hoàn toàn m gam hỗn hợp A gồm xenlulozo, tinh bột, glucozo và saccarozo cần 2,52 lít O2 (đktc) thu được 1,8 gam H2O. Giá trị của m là
- A 5,25.
- B 6,20.
- C 3,60.
- D 3,15.
Đáp án: D
Phương pháp giải:
PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
+ Khi đốt cháy một cacbohidrat ta luôn thu được: nCO2 = nO2
+ Bảo toàn khối lượng: mA = mCO2 + mH2O - mO2
Lời giải chi tiết:
PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
+ Khi đốt cháy một cacbohidrat ta luôn thu được: nCO2 = nO2 = 0,1125 mol
+ Bảo toàn khối lượng: mA = mCO2 + mH2O - mO2 = 0,1125.44 + 1,8 - 0,1125.32 = 3,15 gam
Đáp án D
Câu hỏi 2 :
Đốt cháy hoàn toàn m gam hỗn hợp gồm glucozơ, saccarozơ, xenlulozơ thu được 15,84 gam CO2 và 6,21 gam H2O. Giá trị của m là
- A 10,53.
- B 10,80.
- C 12,25.
- D 12,32.
Đáp án: A
Phương pháp giải:
PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
+ Khi đốt cháy một cacbohidrat ta luôn thu được: nCO2 = nO2
+ Bảo toàn khối lượng: mcacbohidrat = mCO2 + mH2O - mO2
Lời giải chi tiết:
PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
+ Khi đốt cháy một cacbohidrat ta luôn có: nO2 = nCO2 = 0,36 mol
+ Bảo toàn khối lượng: m = mCO2 + mH2O - mO2 = 15,84 + 6,21 - 0,36.32 = 10,53 gam
Đáp án A
Câu hỏi 3 :
Đốt cháy hoàn toàn (m) gam một cacbohiđrat (X) cần 13,44 lít O2 (đktc) sau đó đem hấp thụ hoàn toàn sản phẩm cháy trong 200 ml dung dịch chứa đồng thời NaOH 1,75M và Ba(OH)2 1M thu được kết tủa có khối lượng là
- A 9,85 gam.
- B 39,4 gam.
- C 19,7 gam.
- D 29,55 gam.
Đáp án: D
Phương pháp giải:
+ PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
Khi đốt cháy cacbohidrat ta luôn có: nO2 = nCO2
+ Bài toán trở thành bài toán hấp thụ CO2 vào dd kiềm.
Lời giải chi tiết:
PTHH tổng quát khi đốt cacbohidrat: Cn(H2O)m + nO2 → nCO2 + mH2O
Như vậy, khi đốt cháy cacbohidrat ta luôn có: nO2 = nCO2 = 0,6 mol
Bài toán hấp thụ CO2 vào dd kiềm: \(\left\{ \begin{array}{l}{n_{CO2}} = 0,6mol\\{n_{OH - }} = {n_{NaOH}} + 2{n_{Ba\left( {OH} \right)2}} = 0,75mol\end{array} \right.\)
Tỉ lệ: \(\frac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = \frac{{0,75}}{{0,6}} = 1,25\) => Tạo CO32- và HCO3-
PT ion:
CO2 + 2OH- → CO32- + H2O
x 2x x
CO2 + OH- → HCO3-
y y y
Ta có hệ phương trình: \(\left\{ \begin{array}{l}{n_{C{O_2}}} = x + y = 0,6\\{n_{O{H^ - }}} = 2x + y = 0,75\end{array} \right. \to \left\{ \begin{array}{l}x = 0,15\\y = 0,45\end{array} \right.\)
PT tạo kết tủa:
Ba2+ + CO32- → BaCO3
Bđ: 0,2 0,15
Pư: 0,15 ← 0,15 → 0,15
=> m kết tủa = mBaCO3 = 0,15.197 = 29,55 gam
Đáp án D
Câu hỏi 4 :
Đốt cháy hoàn toàn hỗn hợp X gồm: glucozo; fructozo; metanal; axit etanoic cần 3,36 lít O2 (đktc). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư sau phản ứng hoàn toàn thu được m gam kết tủa. Giá trị của m là
- A 15,0.
- B 12,0.
- C 10,0.
- D 20,5.
Đáp án: A
Phương pháp giải:
+ X đều có dạng (CH2O)n => Quy đổi về CH2O
PT đốt cháy: CH2O + O2 → CO2 + H2O
=> nCO2 = nO2
+ nCaCO3 = nCO2
Lời giải chi tiết:
X: C6H12O6; CH2O; C2H4O2
Ta thấy các chất trong X đều có dạng (CH2O)n => Quy đổi về CH2O
CH2O + O2 → CO2 + H2O
=> nCO2 = nO2 = 0,15 mol
Cho CO2 vào dung dịch Ca(OH)2 dư => mCaCO3 = nCO2 = 0,15 mol
=> mCaCO3 = 15 gam
Đáp án A
Câu hỏi 5 :
Đốt cháy hoàn toàn 9 gam cacbohiđrat X cần 6,72 lít O2 thu được CO2 và H2O. Hấp thụ hết sản phẩm bằng 500ml dd Ba(OH)2 thì thấy khối lượng dd giảm 1,1 gam. Vậy nồng độ mol/l của dung dịch Ba(OH)2 là
- A 0,2M.
- B 0,3M.
- C 0,8M.
- D 0,4M.
Đáp án: D
Phương pháp giải:
+ Bảo toàn khối lượng: mX + mO2 = mCO2 + mH2O
+ Khối lượng dung dịch giảm: ∆ = m kết tủa – (mCO2 + mH2O)
+ Đốt cháy hợp chất có CTTQ: Cn(H2O)m luôn có: nCO2 = nO2
+ Bảo toàn nguyên tố
Lời giải chi tiết:
nO2 = 0,3 mol
BTKL phản ứng cháy: mX + mO2 = mCO2 + mH2O = 18,6 gam
Mặt khác, m dd giảm = m kết tủa – (mCO2 + mH2O) => m kết tủa = 1,1 + 18,6 = 19,7 gam
=> n kết tủa = 0,1 mol
X có công thức dạng Cn(H2O)m
Cn(H2O)m + nO2 → nCO2 + mH2O
nCO2 = nO2 = 0,3 mol > n kết tủa
=> dd có Ba(HCO3)2
BTNT "C" => nCO2 = nBaCO3 + 2nBa(HCO3)2 => nBa(HCO3)2 = 0,1 mol
BTNT "Ba" => nBa(OH)2 = nBaCO3 + nBa(HCO3)2 => nBa(OH)2 = 0,2 mol
=> CM = 0,4M
Đáp án D
Câu hỏi 6 :
Đốt cháy a gam cacbohiđrat cần 6,72 lít O2 sau phản ứng thu được CO2 và H2O. Hấp thụ hết sản phẩm vào dd nước vôi trong dư thì thấy khối lượng dd giảm 11,4 gam. X thuộc loại
- A polisaccarit.
- B monosaccarit.
- C đisaccarit.
- D trisaccarit.
Đáp án: B
Phương pháp giải:
+ Đốt cháy hợp chất có CTTQ: Cn(H2O)m luôn có: nCO2 = nO2
+ Khối lượng dung dịch giảm: ∆ = m kết tủa – (mCO2 + mH2O)
+ Lập tỉ lệ n : m = nCO2 : nH2O
Lời giải chi tiết:
nO2 = 0,3 mol
X có công thức dạng Cn(H2O)m
Cn(H2O)m + nO2 → nCO2 + mH2O
=> nCO2 = nO2 = 0,3 mol
Do Ca(OH)2 dư do đó toàn bộ CO2 được chuyển thành CaCO3
m dd giảm = m CaCO3 – (mCO2 + mH2O)
=> 11,4 = 0,3.100 - (0,3.44 + mH2O) => mH2O = 5,4 gam
=> nH2O = 0,3 mol
=> n : m = nCO2 : nH2O = 1 : 1
Đáp án B
Câu hỏi 7 :
Đốt cháy a gam glucozo sau đó cho toàn bộ sản phẩm cháy hấp thụ hết vào 1 lít dung dịch nước vôi trong có nồng độ 0,39M thu được a gam kết tủa. Giá trị của a là
- A 21,9 gam.
- B 22,5 gam.
- C 15,0 gam.
- D 18,0 gam.
Đáp án: D
Phương pháp giải:
nC6H12O6 = a/180 (mol); nCa(OH)2 = 0,39 (mol); nCaCO3 = a/100 (mol)
C6H12O6 + 6O2 → 6CO2 + 6H2O
a/180 → a/30 (mol)
Ta thấy: nCO2 > nCaCO3 và CO2 được hấp thụ hết vào dd Ca(OH)2 => Phản ứng có tạo Ca(HCO3)2
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 - nCaCO3 (theo ẩn a)
BTNT "C" lập phương trình ẩn a: nCO2 = nCaCO3 + 2nCa(HCO3)2
=> a
Lời giải chi tiết:
nC6H12O6 = a/180 (mol); nCa(OH)2 = 0,39 (mol); nCaCO3 = a/100 (mol)
C6H12O6 + 6O2 → 6CO2 + 6H2O
a/180 → a/30 (mol)
Ta thấy: nCO2 > nCaCO3 và CO2 được hấp thụ hết vào dd Ca(OH)2 => Phản ứng có tạo Ca(HCO3)2
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 - nCaCO3 = 0,39 - a/100 (mol)
BTNT "C": nCO2 = nCaCO3 + 2nCa(HCO3)2
=> \(\frac{a}{{30}} = \frac{a}{{100}} + 2.(0,39 - \frac{a}{{100}})\) => a = 18 gam
Đáp án D
Câu hỏi 8 :
Đốt cháy một lượng gluxit B thu được 2,64 gam CO2 và 1,08 gam nước. B là
- A saccarozo.
- B tinh bột.
- C xenlulozo.
- D fructozo.
Đáp án: D
Phương pháp giải:
+ Viết PTHH: Cn(H2O)m + nO2 → nCO2 + mH2O
+ Lập tỉ lệ H2O : CO2
Lời giải chi tiết:
Ta có: nCO2 = 0,06 mol; nH2O = 0,06 mol
B có công thức dạng Cn(H2O)m
Cn(H2O)m + nO2 → nCO2 + mH2O
0,06 0,06
=> n : m = 0,06 : 0,06 = 1:1
Đáp án D
Câu hỏi 9 :
Hỗn hợp X gồm glucozo và tinh bột. Chia X làm 2 phần bằng nhau.
Phần 1 cho phản ứng với dung dịch AgNO3/NH3 dư tạo ra 3,24 gam Ag.
Phần 2 đem thủy phân hoàn toàn bằng dung dịch H2SO4 loãng rồi trung hòa axit dư bằng dung dịch NaOH, sau đó cho toàn bộ sản phẩm tác dụng với dung dịch AgNO3/NH3 tạo ra 9,72 gam Ag.
Khối lượng tinh bột trong X là
- A 7,29.
- B 14,58.
- C 9,72.
- D 4,86.
Đáp án: C
Phương pháp giải:
+ Phần 1: nGlu = ½nAg
+ Phần 2: Thủy phân tinh bột thu được glucozo => nAg = 2nGlucose + 2nC6H10O5
Lời giải chi tiết:
Phần 1: Chỉ có glucozo phản ứng tráng bạc => nGlucozo = 0,015 mol
Phần 2: Tinh bột thủy phân tạo glucozo => Phản ứng tráng bạc có
n Ag = 2nGlucozo + 2nC6H10O5
=> nC6H10O5 = 0,03 mol
Trong toàn bộ X có 0,06 mol C6H10O5
=> m tinh bột = m C6H10O5 = 9,72 gam
Đáp án C
Câu hỏi 10 :
Đốt cháy một lượng gluxit B thu được 2,64g CO2 và 1,08 g nước. Xác định B
- A Saccarozo
- B Tinh bột
- C Xenlulozo
- D Fructozo
Đáp án: D
Lời giải chi tiết:
Đáp án D
Câu hỏi 11 :
Đốt cháy 24,48 gam hỗn hợp X gồm glucozơ và saccarozơ cần dùng 0,84 mol O2. Mặt khác, nếu đun 24,48 gam X trong môi trường axit, thu được hỗn hợp Y. Trung hòa Y, rồi cho tác dụng với lượng dư dung dịch AgNO3 trong NH3 đun nóng, thu được m gam Ag. Các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
- A 30,24.
- B 25,92.
- C 34,56.
- D 43,20.
Đáp án: A
Phương pháp giải:
Saccarozo→glucose+fructose →4Ag
Glucose → 2Ag
Lời giải chi tiết:
Hướng dẫn giải
Trong X đặt glucose : x mol và saccarzo : y mol
Khối lượng X là 24,48 = 180x + 342y
Đốt cháy X
C6H12O6 +6 O2 → 6CO2 +6H2O
C12H22O11 + 12O2→ 12CO2 + 11H2O
Lượng O2 pư là 6x + 12y = 0,84
→ x=0,06, y=0,04 mol
0,06 mol glucose → 0,12 mol Ag
0,04 mol saccarozo → 0,08 mol glucose → 0,16 mol Ag
→m =0,28.108=30,24
Đáp án A
Câu hỏi 12 :
Hỗn hợp X gồm các chất hữu cơ có công thức phân tử là C3H6O, C6H12O6. Đốt cháy hoàn toàn một lượng hỗn hợp X thì thu được 5,4g H2O và V lit khí CO2 (dktc). Giá trị của V là :
- A 6,72
- B 3,36
- C 5,04
- D 11,20
Đáp án: A
Phương pháp giải:
2 công thức ban đầu đều có số nguyên tử H gấp 2 lần nguyên tử C => nCO2 = nH2O
Lời giải chi tiết:
Do trong C3H6O và C6H12O6 đều có số nguyên tử H gấp đôi số C => nCO2 = nH2O
=> VCO2 = 0,3.22,4 = 6,72 lit
Đáp án A
Câu hỏi 13 :
Đốt cháy hoàn toàn một lượng hỗn hợp X chứa glucozơ và fructozơ, saccarozơ, mantozơ cân dùng vừa đủ 37,632 lít khí O2 (đktc) thu được CO2 và H2O. Cho toàn bộ sản phẩm cháy qua dung dịch Ba(OH)2 dư thấy có m gam kết tủa xuất hiện. Giá trị của m là
- A 260,04.
- B 287,62.
- C 330,96.
- D 220,64.
Đáp án: C
Phương pháp giải:
Quy về CTTQ CnH2nO
nC = nO2
Lời giải chi tiết:
C6H12O6 và C12H22O11 đều có CTTQ CnH2nOn
CnH2nOn + nO2 → nCO2 + nH2O
nCO2 = n O2 = 1,68 (mol)
=> m BaCO3 = 1,68.197 =330, 96 (g)
Đáp án C
Câu hỏi 14 :
Đốt cháy hoàn toàn hỗn hợp chứa glucozo, metyl fomat và saccarozo cần vừa đủ 6,72 lít khí O2 (đktc). Hấp thụ toàn bộ sản phẩm cháy bằng dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
- A 22
- B 25
- C 30.
- D 27.
Đáp án: C
Phương pháp giải:
C6H12O6, C2H4O2, C12H22O11. Quy đổi thành CnH2mOm
Viết PTHH, nhận thấy mối liên hệ giữa số mol O2 và CO2.
Lời giải chi tiết:
C6H12O6, C2H4O2, C12H22O11. Quy đổi thành CnH2mOm
CnH2mOm + nO2 → nCO2 + mH2O
Ta thấy nCO2 = nO2 = 0,3 mol => mCaCO3 = 0,3.100 = 30 gam
Đáp án C
Câu hỏi 15 :
Đốt cháy hoàn toàn hỗn hợp X gồm metanal, axit etanoic, glucozơ và fructozơ cần 7,28 lít khí O2 (đktc). Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư, sau phản ứng thu được kết tủa và dung dịch Y. Khối lượng dung dịch Y so với khối lượng dung dịch Ca(OH)2 ban đầu đã thay đổi như thế nào?
- A Giảm 12,35 gam.
- B Tăng 12,35 gam.
- C Tăng 6,50 gam.
- D Giảm 6,50 gam.
Đáp án: A
Phương pháp giải:
+ Các chất trong X đều có CT dạng: (CH2O)n. Do đó khi đốt cháy ta có: nCO2 = nH2O = nO2.
+ Dẫn sản phẩm cháy (CO2, H2O) qua dung dịch Ca(OH)2 dư:
mdd sau – mdd đầu = (mCO2 + mH2O) – mCaCO3
Lời giải chi tiết:
+ NX: HCHO, CH3COOH, C6H12O6 (glucozơ), C6H12O6 (fructozơ) đều có CT dạng CnH2nOn.
+ Đốt cháy hỗn hợp X:
\(\begin{array}{l}{n_{{O_2}}} = 0,325\,mol\\{C_n}{H_{2n}}{O_n} + n{O_2} \to nC{O_2} + n{H_2}O\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,325\,\, \to \,0,325\,\,\,\,\,\,0,325\,\,\,(mol)\end{array}\)
+ Vì dung dịch Ca(OH)2 dư nên nCaCO3 = nCO2 = 0,325 mol → mCaCO3 = 32,5 gam.
Ta có: mdd sau – mdd đầu = (mCO2 + mH2O) – mCaCO3 = 0,325.44 + 0,325.18 – 32,5 = – 12,35 gam < 0
→ dung dịch Y so với dung dịch Ca(OH)2 ban đầu đã giảm đi 12,35 gam.
Đáp án A
Câu hỏi 16 :
Chia hỗn hợp X gồm glucozơ, fructozơ, saccarozơ và tinh bột thành 2 phần bằng nhau. Đốt cháy hoàn toàn phần một cần vừa đủ 8,736 lít khí O2 (đktc), thu được CO2 và H2O. Thủy phân hoàn toàn phần hai trong môi trường axit, thu được dung dịch T. Trung hòa T bằng kiềm rồi cho tác dụng hết với lượng dư dung dịch AgNO3 trong NH3 (đun nhẹ) thu được m gam Ag. Giá trị của m là
- A 21,06.
- B 21,60.
- C 14,04.
- D 10,80.
Đáp án: C
Phương pháp giải:
Hỗn hợp X gồm các chất đều có dạng Cn(H2O)m và khi đốt cháy ta thấy nO2 = nCO2 = nC(X). (1)
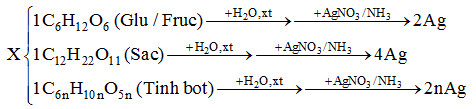
(Để đơn giản hơn, ta có thể coi số mắt xích của tinh bột n = 1)
Ta thấy: nAg = 1/3. nC(X) (2). Từ (1) và (2) → số mol Ag.
Lời giải chi tiết:
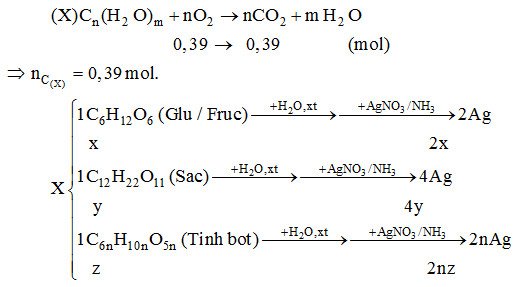
\( \Rightarrow {n_{Ag}} = 2x + 4y + 2nz = \frac{1}{3}{n_{{C_{(X)}}}} = 0,13\,mol \Rightarrow {m_{Ag}} = 14,04\,gam.\)
Đáp án C
Câu hỏi 17 :
Một mẩu saccarozo có lẫn một lượng nhỏ glucozo. Đem đốt cháy hoàn toàn lượng chất rắn này rồi cho toàn bộ sản phẩm cháy lội qua 300 ml dung dịch Ba(OH)2 2M, thu được 59,1 gam kết tủa, tiếp tục đung nóng dung dịch sau phản ứng lại thu thêm kết tủa. Nếu thủy phân hoàn toàn mẫu vật trên trong môi trường axit, sau đó trung hòa dung dịch rồi cho tác dụng với lượng dư AgNO3 trong dung dịch NH3, đun nhẹ đến khi phản ứng xảy ra hoàn toàn thu được m gam Ag. Giá trị của m là
- A 32,4.
- B 21,6.
- C 10,8.
- D 64,8.
Đáp án: A
Phương pháp giải:
* Đốt cháy chất rắn và dẫn sản phẩm qua dung dịch Ba(OH)2:
Tính được: nBa(OH)2 = ? và nBaCO3 = ?
Do tiếp tục đun nóng dung dịch lại thu được kết tủa nên dung dịch có chứa muối Ba(HCO3)2
BTNT “Ba” => nBa(HCO3)2 = nBa(OH)2 – nBaCO3 = ?
BTNT “C”: nCO2 = nBaCO3 + 2nBa(HCO3)2 = ?
* Thủy phân chất rắn trong môi trường axit rồi cho sản phẩm tráng bạc:
BT “C” => nC6H12O6 = nCO2/6 = ?
=> nAg = 2nC6H12O6 = ?
=> m = ?
Lời giải chi tiết:
* Đốt cháy chất rắn và dẫn sản phẩm qua dung dịch Ba(OH)2:
nBa(OH)2 = 0,6 mol
nBaCO3 = 0,3 mol
Do tiếp tục đun nóng dung dịch lại thu được kết tủa nên dung dịch có chứa muối Ba(HCO3)2
BTNT “Ba” => nBa(HCO3)2 = nBa(OH)2 – nBaCO3 = 0,6 – 0,3 = 0,3 mol
BTNT “C”: nCO2 = nBaCO3 + 2nBa(HCO3)2 = 0,3 + 2.0,3 = 0,9 mol
* Thủy phân chất rắn trong môi trường axit rồi cho sản phẩm tráng bạc:
BT “C” => nC6H12O6 = nCO2/6 = 0,9:6 = 0,15 mol
=> nAg = 2nC6H12O6 = 0,3 mol
=> m = 0,3.108 = 32,4 gam
Đáp án A
Câu hỏi 18 :
Đốt cháy hoàn toàn m gam hỗn hợp X tinh bột, glucozơ và saccarozơ cần 16,8 lít O2(đktc), thu được hỗn hợp Y gồm khí cacbonic và hơi nước. Hấp thụ hoàn toàn Y vào dung dịch nước vôi trong (dư) thu được x gam kết tủa.Giá trị của x là
- A 22,5.
- B 15,0.
- C 75,0.
- D 45,0.
Đáp án: C
Phương pháp giải:
BTNT “C”: nCaCO3 = nCO2 = nC = nO2= ?(mol)
Lời giải chi tiết:
nO2(ĐKTC) = 16,8 : 22,4 = 0,75 (mol)
Gọi công thức chung của X là: Cn(H2O)m
Đốt X thực chất là quá trình đốt Cacbon
C + O2 → CO2
0,75← 0,75 (mol)
BTNT “C”: nCaCO3 = nCO2 = nC = 0,75 (mol)
=> mCaCO3 = 0,75.100 = 75 (g)
Đáp án C
Câu hỏi 19 :
Đốt cháy hoàn toàn một lượng hỗn hợp X gồm glucozo, fructozo, saccarozo cần dùng vừa đủ 37,632 lít khí O2(đktc) thu được CO2 và H2O. Cho toàn bộ lượng sản phẩm cháy qua dung dịch Ba(OH)2 thấy có m gam kết tủa xuất hiện. Giá trị của m là
- A 287,62.
- B 260,04.
- C 220,64.
- D 330,96.
Đáp án: D
Phương pháp giải:
Đặt công thức chung của X là Cn(H2O)m
Đốt X thực chất là đốt C vì chỉ có C cháy: C + O2 → CO2
BTNT: nBaCO3 = nC = nO2 = 1,68 (mol)
Lời giải chi tiết:
Đặt công thức chung của X là Cn(H2O)m
nO2(đktc) = 37,632 :22,4 = 1,68 (mol)
Đốt X thực chất là đốt C vì chỉ có C cháy
C + O2 → CO2
BTNT: nBaCO3 = nC = nO2 = 1,68 (mol)
=> m↓ = mBaCO3 = 1,68.197 = 330,96 (g)
Đáp án D
Câu hỏi 20 :
Đốt cháy hoàn toàn 0,15 mol hỗn hợp X gồm glucozơ, xenlulozơ, saccarozơ cần dùng 1,02 mol O2, thu được CO2 và H2O có tổng khối lượng là 61,98 gam. Nếu cho 0,15 mol X trên vào lượng dư dung dịch AgNO3 trong NH3 đun nóng, thu được m gam Ag. Giá trị của m là
- A 25,92.
- B 17,28.
- C 21,60.
- D 36,72.
Đáp án: B
Phương pháp giải:
Đặt a,b, c là số mol glucozơ (C6H12O6 = C6(H2O)6 ), saccarozơ (C12H22O11 = C11(H2O)11) và xenlulozơ (C6H10O5)n = C6(H2O)5
nX = a + b + c = 0,15
Đốt X thực chất là đốt cháy C
nCO2 = nO2 = 1,02 (mol)
=> 6a + 12b + 6c = 1,02 (2)
mCO2 + mH2O = 1,02.44 + 18.(6a +11b + 5c) = 61,98 (3)
Giải hệ (1), (2), (3) => a = ? ; b = ? và c = ? (mol)
Cho X tác dụng với dd AgNO3/NH3 chỉ có glucozo tham gia phản ứng
Lời giải chi tiết:
Đặt a,b, c là số mol glucozơ (C6H12O6 = C6(H2O)6 ), saccarozơ (C12H22O11 = C11(H2O)11) và xenlulozơ (C6H10O5)n = C6(H2O)5
nX = a + b + c = 0,15
CT chung của X có dạng Cn(H2O)m: 0,1 mol Đốt X thực chất là đốt cháy C
C + O2 → CO2
nCO2 = nO2 = 1,02 (mol)
=> 6a + 12b + 6c = 1,02 (2)
mCO2 + mH2O = 1,02.44 + 18.(6a +11b + 5c) = 61,98 (3)
Giải hệ (1), (2), (3) => a = 0,08 ; b = 0,02 và c = 0,05 (mol)
Cho X tác dụng với dd AgNO3/NH3 chỉ có glucozo tham gia phản ứng
=> nAg = 2nGlu = 2a = 0,16 (mol)
=> mAg = 0,6.108 = 17,28 (g)
Đáp án B
Câu hỏi 21 :
Đốt cháy hoàn toàn một hỗn hợp X: axit axetic, andehit fomic, glucozo và fructozo cần 3,36 lít O2(đktc). Hấp thụ sản phẩm cháy vào dung dịch Ca(OH)2 dư. Khối lượng dung dịch Ca(OH)2 thay đổi như thế nào?
- A Tăng 9,3 gam.
- B Tăng 6,6 gam.
- C Giảm 5,7 gam.
- D Giảm 12,3 gam.
Đáp án: C
Phương pháp giải:
Hỗn hợp X gồm: C2H4O2; CH2O; C6H12O6; C6H12O6 → tất cả các chất này có công thức chung là (CH2O)n
PTHH: (CH2O)n + nO2 → nCO2 + nH2O
→ nCO2 = nH2O = 0,15 (mol)
Khi cho sp cháy vào dd Ca(OH)2 dư có phản ứng
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,15 → 0,15 (mol)
Xét: ∆m = mCO2 + mH2O - mCaCO3 = ?
∆m > 0 thì khối lượng dd tăng; ∆m < 0 thì khối lượng dung dịch giảm
Lời giải chi tiết:
Hỗn hợp X gồm: C2H4O2; CH2O; C6H12O6; C6H12O6 → tất cả các chất này có công thức chung là (CH2O)n
nO2(đktc) = 3,36 : 22,4 = 0,15 (mol)
PTHH: (CH2O)n + nO2 → nCO2 + nH2O
0,15 → 0,15 0,15 (mol)
→ nCO2 = nH2O = 0,15 (mol)
Khi cho sp cháy vào dd Ca(OH)2 dư có phản ứng
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,15 → 0,15 (mol)
Xét: ∆m = mCO2 + mH2O - mCaCO3 = 0,15.44 + 0,15.18 - 0,15.100 = -5,7
Vậy khối lượng dung dịch Ca(OH)2 giảm 5,7 g
Đáp án C
Câu hỏi 22 :
Đốt cháy hoàn toàn 1 cacbohiđrat X rồi dẫn toàn bộ sản phẩm cháy vào bình nước vôi trong thì thu được kết tủa và dung dịch Y; khối lượng bình tăng và khối lượng dung dịch tăng lần lượt là 3,63 gam và 0,63 gam. Đun sôi dung dịch Y lại thấy xuất hiện kết tủa. Tổng khối lượng kết tủa của cả hai lần là 4,5 gam. X có thể là
- A Tinh bột.
- B Glucozo.
- C Xenlulozo.
- D Saccarozo.
Đáp án: D
Phương pháp giải:
m dd tăng = mCO2 + mH2O
m bình tăng = mCO2 + mH2O – mCaCO3
=> mCaCO3
Do đun nóng dung dịch Y lại thu được kết tủa nên trong Y chứa Ca(HCO3)2
Tính theo PTHH thu được số mol của CaCO3 và Ca(HCO3)2
BTNT “C”: nCO2 = nCaCO3 + 2nCa(HCO3)2
=> mH2O = 3,63 – mCO2 => nH2O => nH
Xác định tỉ lệ C : H => X
Lời giải chi tiết:
m dd tăng = mCO2 + mH2O = 3,63
m bình tăng = mCO2 + mH2O – mCaCO3 = 0,63
=> mCaCO3 = 3 gam
Do đun nóng dung dịch Y lại thu được kết tủa nên trong Y chứa Ca(HCO3)2
=> Khối lượng CaCO3 sinh thêm sau khi đun nóng Y là 4,5 – 3 = 1,5 gam
Ca(HCO3)2 → CaCO3 + CO2 + H2O
0,015 ← 0,015
Như vậy: nCaCO3 = 0,03 mol và nCa(HCO3)2 = 0,015 mol
BTNT “C”: nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,03 + 2.0,015 = 0,06 mol
=> mH2O = 3,63 – mCO2 = 3,63 – 0,06.44 = 0,99 gam => nH2O = 0,055 mol
=> nH = 2nH2O = 0,11 mol
C : H = 0,06 : 0,11 = 6 : 11
=> X là C12H22O11 (Saccarozo)
Đáp án D
Câu hỏi 23 :
Đốt cháy hoàn toàn 15,48 gam hỗn hợp gồm glucozơ, saccarozơ và xenlulozơ cần dùng 0,54 mol O2, sản phẩm cháy dẫn qua dung dịch Ca(OH)2 dư, thu được dung dịch có khối lượng giảm m gam so với dung dịch ban đầu. Giá trị m là
- A 21,24 gam.
- B 23,04 gam.
- C 19,44 gam.
- D 22,14 gam.
Đáp án: A
Phương pháp giải:
- Khi đốt cacbohiđrat ta luôn có: nCO2 = nO2 (HS chứng minh bằng cách viết PTHH)
- Bảo toàn khối lượng tính khối lượng H2O
- Khi đưa sp cháy qua bình Ca(OH)2 thì CO2, H2O bị hấp thụ và có phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
Khối lượng dung dịch giảm: mdd giảm = mmất đi - mthêm vào = mCaCO3 - (mCO2 + mH2O)
Lời giải chi tiết:
- Khi đốt cacbohiđrat ta luôn có: nCO2 = nO2 = 0,54 mol
- Bảo toàn khối lượng ⟹ mH2O = mhỗn hợp + mO2 - mCO2 = 15,48 + 0,54.32 - 0,54.44 = 9 gam
- Khi đưa sp cháy qua bình Ca(OH)2 thì CO2, H2O bị hấp thụ và có phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,54 → 0,54 (mol)
Khối lượng dung dịch giảm:
mdd giảm = mmất đi - mthêm vào = mCaCO3 - (mCO2 + mH2O) = 0,54.100 - (0,54.44 + 9) = 21,24 gam
Đáp án A
Câu hỏi 24 :
Đốt cháy hoàn toàn 9,0 gam cacbohiđrat X cần 6,72 lít O2 (đktc) thu được CO2 và H2O. Hấp thụ hết sản phẩm cháy bằng 250 ml dung dịch Ba(OH)2 thì thấy khối lượng dung dịch giảm 1,1 gam. Nồng độ mol/l của dung dịch Ba(OH)2 là
- A 0,2M.
- B 0,3M.
- C 0,4M.
- D 0,8M.
Đáp án: D
Phương pháp giải:
Đốt cacbohidrat luôn có: nCO2 = nO2 = ? (mol) ⟹ mCO2 = nCO2×MCO2 = ?(g)
BTKL ta có: mX + mO2 = mCO2 + mH2O ⟹ mH2O = ? (g) ⟹ nH2O = mH2O : nH2O = ? (mol)
Sản phẩm cháy hấp thụ vào dd Ba(OH)2 có:
mdd giảm = mBaCO3 – (mCO2 + mH2O) ⟹ mBaCO3 = ? (g)⟹ nBaCO3 = ? (mol)
Hấp thụ CO2 vào dd Ba(OH)2 tạo ra 2 muối BaCO3 và Ba(HCO3)2
BTNT “Ba”: nBa(OH)2 = nBaCO3 + nBa(HCO3)2 = ?
Lời giải chi tiết:
nO2(đktc) = VO2/22,4 = 0,3 (mol)
Đặt công thức cacbohiđrat có dạng: Cn(H2O)m
PT cháy: Cn(H2O)m + nO2 nCO2 + mH2O
Theo PTHH ta thấy: nCO2 = nO2 = 0,3 (mol) ⟹ mCO2 = nCO2×MCO2 = 0,3×44 = 13,2 (g)
BTKL ta có: mX + mO2 = mCO2 + mH2O
⟹ 9 + 0,3× 32 = 13,2+ mH2O
⟹ mH2O = 5,4 (g)
⟹ nH2O = mH2O : nH2O = 5,4 : 18 = 0,3 (mol)
Sản phẩm cháy hấp thụ vào dd Ba(OH)2 có:
mdd giảm = mBaCO3 – (mCO2 + mH2O)
⟹ 1,1 = mBaCO3 – (13,2 + 5,4)
⟹ mBaCO3 = 19,7 (g)
⟹ nBaCO3 = mBaCO3 : MBaCO3 = 19,7 : 197 = 0,1 (mol)
Hấp thụ CO2 vào dd Ba(OH)2 tạo ra 2 muối BaCO3 và Ba(HCO3)2
BTNT “C”: nCO2 = 2nBa(HCO3)2 + nBaCO3 ⟹ nBa(HCO3)2 = (nCO2 – nBaCO3)/2 = (0,3 – 0,1)/2 = 0,1 (mol)
BTNT “Ba”: nBa(OH)2 = nBaCO3 + nBa(HCO3)2 = 0,1 + 0,1 = 0,2 (mol)
⟹ CM Ba(OH)2 = nBa(OH)2 : VBa(OH)2 = 0,2 : 0,25 = 0,8 (M)
Đáp án D
Câu hỏi 25 :
Đốt cháy hoàn toàn m gam hỗn hợp X gồm glucozơ, saccarozơ và xenlulozơ trong oxi dư, sau phản ứng thu được 53,76 lít CO2 (đktc) và 39,6 gam H2O. Giá trị của m là
- A 51,30.
- B 61,55.
- C 68,40.
- D 54,72.
Đáp án: C
Phương pháp giải:
Khi đốt cacbohiđrat luôn có mối liên hệ nO2 = nCO2
Bảo toàn khối lượng tính được m
Lời giải chi tiết:
Khi đốt cacbohiđrat luôn có mối liên hệ nO2 = nCO2 = 53,76/22,4 = 2,4 mol
(HS tự chứng minh bằng cách viết PTHH đốt cháy Cn(H2O)m)
BTKL: mX + mO2 = mCO2 + mH2O
⇔ m + 2,4.32 = 2,4.44 + 39,6
⇔ m = 68,4 gam
Đáp án C
Câu hỏi 26 :
Một mẩu saccarozo có lẫn một lượng nhỏ glucozo. Đem đốt cháy hoàn toàn lượng chất rắn này rồi cho toàn bộ sản phẩm cháy lội qua 300 ml dung dịch Ba(OH)2 2M, thu được 59,1 gam kết tủa, tiếp tục đung nóng dung dịch sau phản ứng lại thu thêm kết tủa. Nếu thủy phân hoàn toàn mẫu vật trên trong môi trường axit, sau đó trung hòa dung dịch rồi cho tác dụng với lượng dư AgNO3 trong dung dịch NH3, đun nhẹ đến khi phản ứng xảy ra hoàn toàn thu được m gam Ag. Giá trị của m là
- A 32,4.
- B 21,6.
- C 10,8.
- D 64,8.
Đáp án: A
Phương pháp giải:
* Đốt cháy chất rắn và dẫn sản phẩm qua dung dịch Ba(OH)2:
Tính được: nBa(OH)2 = ? và nBaCO3 = ?
Do tiếp tục đun nóng dung dịch lại thu được kết tủa nên dung dịch có chứa muối Ba(HCO3)2
BTNT “Ba” => nBa(HCO3)2 = nBa(OH)2 – nBaCO3 = ?
BTNT “C”: nCO2 = nBaCO3 + 2nBa(HCO3)2 = ?
* Thủy phân chất rắn trong môi trường axit rồi cho sản phẩm tráng bạc:
BT “C” => nC6H12O6 = nCO2/6 = ?
=> nAg = 2nC6H12O6 = ?
=> m = ?
Lời giải chi tiết:
* Đốt cháy chất rắn và dẫn sản phẩm qua dung dịch Ba(OH)2:
nBa(OH)2 = 0,6 mol
nBaCO3 = 0,3 mol
Do tiếp tục đun nóng dung dịch lại thu được kết tủa nên dung dịch có chứa muối Ba(HCO3)2
BTNT “Ba” => nBa(HCO3)2 = nBa(OH)2 – nBaCO3 = 0,6 – 0,3 = 0,3 mol
BTNT “C”: nCO2 = nBaCO3 + 2nBa(HCO3)2 = 0,3 + 2.0,3 = 0,9 mol
* Thủy phân chất rắn trong môi trường axit rồi cho sản phẩm tráng bạc:
BT “C” => nC6H12O6 = nCO2/6 = 0,9:6 = 0,15 mol
=> nAg = 2nC6H12O6 = 0,3 mol
=> m = 0,3.108 = 32,4 gam
Đáp án A
Câu hỏi 27 :
Một mẩu saccarozo có lẫn một lượng nhỏ glucozo. Đem đốt cháy hoàn toàn lượng chất rắn này rồi cho toàn bộ sản phẩm cháy lội qua 300 ml dung dịch Ba(OH)2 2M, thu được 59,1 gam kết tủa, tiếp tục đung nóng dung dịch sau phản ứng lại thu thêm kết tủa. Nếu thủy phân hoàn toàn mẫu vật trên trong môi trường axit, sau đó trung hòa dung dịch rồi cho tác dụng với lượng dư AgNO3 trong dung dịch NH3, đun nhẹ đến khi phản ứng xảy ra hoàn toàn thu được m gam Ag. Giá trị của m là
- A 32,4.
- B 21,6.
- C 10,8.
- D 64,8.
Đáp án: A
Lời giải chi tiết:
* Đốt cháy chất rắn và dẫn sản phẩm qua dung dịch Ba(OH)2:
nBa(OH)2 = 0,6 mol
nBaCO3 = 0,3 mol
Do tiếp tục đun nóng dung dịch lại thu được kết tủa nên dung dịch có chứa muối Ba(HCO3)2
BTNT “Ba” => nBa(HCO3)2 = nBa(OH)2 – nBaCO3 = 0,6 – 0,3 = 0,3 mol
BTNT “C”: nCO2 = nBaCO3 + 2nBa(HCO3)2 = 0,3 + 2.0,3 = 0,9 mol
* Thủy phân chất rắn trong môi trường axit rồi cho sản phẩm tráng bạc:
BT “C” => nC6H12O6 = nCO2/6 = 0,9:6 = 0,15 mol
=> nAg = 2nC6H12O6 = 0,3 mol
=> m = 0,3.108 = 32,4 gam
Đáp án A
Câu hỏi 28 :
Đốt cháy hoàn toàn 11,64 gam hỗn hợp X (glucozơ, fructozơ, metanal, axit axetic, metyl fomilat, saccaroz ơ, tinh bột) cần 8,96 lít O2 đktc. Dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư. Lọc tách kết tủa, thấy khối lượng dung dịch thay đổi bao nhiêu gam so với dung dịch Ca(OH)2 ban đầu
- A tăng 24,44 gam
- B tăng 15,56 gam
- C giảm 15,56 gam
- D Giảm 40,0 gam
Đáp án: C
Phương pháp giải:
Quy về CTTQ: Cn(H2O)m đốt cháy luôn có nO2 = nCO2
Lời giải chi tiết:
nO2 = 8,96: 22,4 = 0,4 mol
Glucozơ và Fructo zơ : C6H12O6 ; metanal : CH2O ; axit axetic: C2H4O; saccarozơ: C12H22O11; tinh bột (C6H10O5)n
=> CTTQ chung Cn(H2O)m
Bản chất đốt cháy các hợp chất này là quá trình đốt cháy cacbon
C+ O2 → CO2
0,4← 0,4→ 0,4
CO2 + Ca(OH)2 dư → CaCO3↓
0,4 → 0,4
Từ CTTQ =>\({n_{{H_2}O}} = \frac{{{m_X} - {m_C}}}{{18}} = \frac{{11,64 - 0,4.12}}{{18}} = 0,38\,\,mol\)
Khối lượng dung dịch sau: ∆ = mCO2 + mH2O – mCaCO3↓
= 0,4.44 + 0,38.18 – 0,4.100 = -15,56
Vậy khối lượng dung dịch sau giảm 15,56 gam so với dung dịch Ca(OH)2 ban đầu
Đáp án C
Câu hỏi 29 :
Đốt cháy hoàn toàn hỗn hợp X metanal, axit axetic, metyl fomat, axit lactic (CH3CH(OH)COOH) và glucozơ cần V lít O2 (đktc). Sản phẩm thu được hấp thụ hết vào dung dịch Ca(OH)2. Sau khi kết thúc phản ứng, thu được 10 gam kết tủa và thấy khối lượng dung dịch sau phản ứng tăng thêm 2,4 gam so với khối lượng nước vôi ban đầu. Giá trị của V là
- A 3,36.
- B 4,48.
- C 1,12.
- D 2,24.
Đáp án: B
Phương pháp giải:
- Ta thấy các chất đều có dạng CnH2nOn nên khi đốt thu được số mol CO2 bằng số mol H2O.
- Công thức khối lượng dung dịch tăng: mdd tăng = (mCO2 + mH2O) - mCaCO3 → tính được lượng CO2, H2O
- Từ công thức phân tử thấy số nguyên tử C bằng số nguyên tử O → lượng O trong X
- Bảo toàn nguyên tố O để tính lượng O2 → giá trị của V
Lời giải chi tiết:
Metanal: HCHO (CH2O)
Axit axetic: CH3COOH (C2H4O2)
Metyl fomat: HCOOCH3 (C2H4O2)
Axit lactic: CH3CH(OH)COOH (C3H6O3)
Glucozơ: C6H12O6
Ta thấy các chất đều có dạng CnH2nOn nên khi đốt thu được số mol CO2 bằng số mol H2O
Giả sử nCO2 = nH2O = x mol
Ta có: mdd tăng = (mCO2 + mH2O) - mCaCO3
→ 2,4 = (44x + 18x) - 10
→ x = 0,2
Vì số nguyên tử C bằng số nguyên tử O → nO(X) = nC = nCO2 = 0,2 mol
Bảo toàn O → nO2 = (2nCO2 + nH2O - nO(X))/2 = (2.0,2 + 0,2 - 0,2)/2 = 0,2 mol
→ V = 4,48 lít
Đáp án B
Câu hỏi 30 :
Đốt cháy hoàn toàn hỗn hợp chứa glucozo, metyl fomat và saccarozo cần vừa đủ 6,72 lít khí O2 (đktc). Hấp thụ toàn bộ sản phẩm cháy bằng dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
- A 25
- B 27.
- C 22
- D 30.
Đáp án: D
Phương pháp giải:
- Hỗn hợp chứa C6H12O6, CH2O, C12H22O11 nên các chất trong hỗn hợp có dạng Cm(H2O)n
- PTHH: Cm(H2O)n + mO2 \(\xrightarrow{{{t^o}}}\)mCO2 + nH2O
- Từ PTHH suy ra mối liên hệ giữa mol O2 và CO2
- Khi hấp thụ sản phẩm cháy vào Ca(OH)2 dư thì: \({n_{CaC{{\text{O}}_3}}} = {n_{C{O_2}}}\)
Lời giải chi tiết:
Hỗn hợp chứa C6H12O6, CH2O, C12H22O11 nên các chất trong hỗn hợp có dạng Cm(H2O)n
PTHH: Cm(H2O)n + mO2 \(\xrightarrow{{{t^o}}}\) mCO2 + nH2O
Từ PTHH ta thấy: \({n_{C{O_2}}} = {n_{{O_2}}} = 0,3(mol)\)
Khi hấp thụ sản phẩm cháy vào Ca(OH)2 dư thì: \({n_{CaC{{\text{O}}_3}}} = {n_{C{O_2}}} = 0,3(mol)\)
→ m = 0,3.100 = 30 gam
Đáp án D
