Câu hỏi 1 :
X là một nguyên tố nguyên tố p. Tổng số hạt trong nguyên tử của nguyên tố X là 40. Vị trí của X trong bảng tuần hoàn là
- A Ô 40, chu kỳ 5, nhóm IVB
- B Ô 14, chu kỳ 3, nhóm IIA.
- C Ô 13, chu kỳ 3, nhóm IIIA
- D Ô 15, chu kỳ 3, nhóm VA.
Đáp án: C
Phương pháp giải:
Đối với các nguyên tố có Z ≤ 82 ta luôn có: \(1 \le \frac{N}{Z} \le 1,5\)
Lời giải chi tiết:
Tổng số hạt của X là 40 => 2Z + N = 40 => N = 40 - 2Z
Đối với các nguyên tố có Z ≤ 82 ta luôn có: \(1 \le \frac{N}{Z} \le 1,5\)
\( \to 1 \le \frac{{40 - 2Z}}{Z} \le 1,5\)
→ Z ≤ 40 – 2Z ≤ 1,5Z
11,43 ≤ Z ≤ 13,33
→ Z = 12 hoặc Z = 13
*Trường hợp 1:
Với Z = 12: X có cấu hình là 1s22s22p63s2 => X là nguyên tố s => loại
*Trường hợp 2:
Với Z = 13: X có cấu hình là 1s22s22p63s23p1 => X là nguyên tố p => thỏa mãn đề bài
Vị trí của X:
- Chu kì 3 (do có 3 lớp e)
- Nhóm IIIA (do là nguyên tố p và có 3e lớp ngoài cùng)
Đáp án C
Câu hỏi 2 :
Hai nguyên tố X và Y thuộc 2 ô liên tiếp trong bảng HTTH (cùng một chu kỳ). Tổng số hạt mang điện trong cả 2 nguyên tử X và Y là 66 hạt (biết ZX<ZY). Hai nguyên tố đó là:
- A S và Cl.
- B P và S.
- C Cl và Ar.
- D Si và P.
Đáp án: A
Phương pháp giải:
- Hai nguyên tố X và Y thuộc 2 ô liên tiếp trong bảng HTTH (cùng một chu kỳ) (ZX<ZY): ZY-ZX = 1
- Tổng số hạt mang điện trong cả 2 nguyên tử X và Y là 66 hạt: 2ZX + 2ZY = 66
Lời giải chi tiết:
X và Y thuộc 2 ô liên tiếp trong HTTH và cùng 1 chu kì => ZY – ZX = 1 (1)
Tổng số hạt mang điện trong cả 2 nguyên tử X và Z là 66 => 2ZX + 2ZY = 66 => ZX + ZY = 33 (2)
Giải hệ (1) và (2) => ZY = 17 và ZX = 16
=> Đáp án A
Câu hỏi 3 :
Hai nguyên tố T và U thuộc cùng một nhóm A và nằm ở 2 chu kỳ liên tiếp. Tổng số protron trong cả hai nguyên tử nguyên tố là 32. Hai nguyên tố T và U lần lượt là (ZT< ZU):
- A Na và K.
- B Mg và Ca.
- C O và S.
- D F và Cl.
Đáp án: B
Phương pháp giải:
- Hai nguyên tố T và U thuộc cùng một nhóm A và nằm ở 2 chu kỳ liên tiếp (ZT<ZU) :
+ TH1 : ZU – ZT = 8
+ TH2 : ZU – ZT = 18
- Tổng số protron trong cả hai nguyên tử nguyên tố là 32: ZU + ZT =32
Lời giải chi tiết:
Tổng số proton của 2 nguyên tử là 32 => ZU + ZT = 32
T và U thuộc cùng 1 nhóm A và nằm ở 2 chu kì kế tiếp xảy ra 2 TH
TH1: ZU – ZT = 8
=> ZU = 20 (Ca) và ZT = 12 (Mg)
Thỏa mãn đề bài
TH2: ZU – ZT = 18
=> ZU = 25 (Mn) và ZT = 7 (N)
U và T không thuộc cùng nhóm A (loại)
=> Đáp án B
Câu hỏi 4 :
X và Y (ZX<ZY) là hai nguyên tố thuộc cùng một nhóm A và hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số hạt proton của hai nguyên tử hai nguyên tố đó là 22. Nhận xét đúng về X,Y là
- A Đơn chất của X tác dụng được với đơn chất củaY.
- B Độ âm điện của Y lớn hơn độ âm điện củaX.
- C Hợp chất của X với hiđro là phân tử phân cực.
- D Công thức oxit cao nhất của Y là YO3.
Đáp án: C
Phương pháp giải:
- Hai nguyên tố X và Y thuộc cùng một nhóm A và nằm ở 2 chu kỳ liên tiếp (ZX<ZY) :
+ TH1 : ZY – ZX = 8
+ TH2 : ZY – ZX = 18
- Tổng số protron trong cả hai nguyên tử nguyên tố là 22: ZY + ZX = 22
Lời giải chi tiết:
X và Y thuộc 2 chu kì liên tiếp trong nhóm A
=> Số proton của Y có thể hơn X 8 hoặc 18 proton ( Do tổng số proton 2 nguyên tử 2 nguyên tố = 22)
+/ Nếu pX + 18 = pY => pX = 2 (He) ; pY = 20 (Ca) => Loại.
+/ Nếu pX + 8 = pY => pX = 7 ; pY = 15
=> X là Nito ; Y là Photpho.
=> Hợp chất X với Hidro là NH3 là phân tử phân cực.
=> Đáp án C
Câu hỏi 5 :
Hai nguyên tố X, Y thuộc cùng nhóm và ở hai chu kỳ liên tiếp nhau có tổng số số hiệu nguyên tử là 32. Vậy X, Y thuộc nhóm nào?
- A VIIA
- B IIIA
- C VIA
- D IIA
Đáp án: D
Phương pháp giải:
- Hai nguyên tố X và Y thuộc cùng một nhóm A và nằm ở 2 chu kỳ liên tiếp (ZX<ZY) :
+ TH1 : ZY – ZX = 8
+ TH2 : ZY – ZX = 18
- Tổng số hiệu nguyên tử là 22: ZY + ZX = 32
Lời giải chi tiết:
Giả sử px < py, ta có px + 8 = py
=> px + px + 8 = 32
=> px = 12 => py = 20
(Mg và Ca)
=> Đáp án D
Câu hỏi 6 :
Nguyên tử nguyên tố X có tổng số electron trong các phân lớp p là 8. Vị trí của X trong bảng hệ thống tuần hoàn là :
- A X có số thứ tự 13, chu kì 3, nhóm IIIA.
- B X có số thứ tự 14, chu kì 3, nhóm IVA.
- C X có số thứ tự 12, chu kì 3, nhóm IIA.
- D X có số thứ tự 15, chu kì 3, nhóm VA.
Đáp án: B
Phương pháp giải:
Viết cấu hình e sao cho tổng e ở phân lớp p là 8 => vị trí của X
Lời giải chi tiết:
Cấu hình e của X là 1s22s22p63s23p2 => có 14e nên ở ô số 14
=> có 4e lớp ngoài cùng => nhóm IV A
Có 3 lớp e => chu kì 3
=> Đáp án B
Câu hỏi 7 :
X và Y là hai nguyên tố thuộc hai nhóm A liên tiếp của cùng 1 chu kì. Biết ZX < ZY và ZX + ZY = 31. Y thuộc nhóm VIA. Kết luận nào sau đây là đúng với X và Y?
- A X và Y đều là kim loại.
- B Ở trạng thái cơ bản Y có một electron độc thân.
- C Ở trạng thái cơ bản X có 3 electron độc thân.
- D Công thức oxit cao nhất của X là XO2.
Đáp án: C
Lời giải chi tiết:
X và Y là hai nguyên tố thuộc hai nhóm A liên tiếp của cùng 1 chu kì → ZY - ZX = 1
Ta giải hệ: ZX + ZY = 31 và ZY - ZX = 1 → X là P và Y là S
Cấu hình e của S: 1s22s22p63s23p4
Cấu hình e của P: 1s22s22p63s23p3
- A sai vì X, Y đều là phi kim
- B sai vì Y có 2e độc thân
- C đúng
- D sai vì công thức oxit cao nhất là P2O5.
Đáp án C
Câu hỏi 8 :
X và Y là 2 nguyên tố thuộc cùng nhóm nhóm IA trong bảng HTTH và ở 2 chu kỳ liên tiếp. Hoà tan hoàn toàn 7,35 gam hỗn hợp này vào nước (dư), sau phản ứng thu được được dung dịch Z và 2,8 lít H2 (đktc). X, Y là
- A Li và Na.
- B Na và K.
- C K và Rb.
- D Rb và Cs.
Đáp án: B
Lời giải chi tiết:
Gọi A là công thức trung bình của X và Y
PTHH: 2A + 2H2O → 2AOH + H2
0,25 ← 0,125 (mol)
=> MA = 7,35 : 0,25 = 29,4
Do X và Y thuộc cùng nhóm IA và ở 2 chu kì liên tiếp nên là Na (M = 23) và K (M = 39)
Đáp án B
Câu hỏi 9 :
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 8. Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhỏ hơn tổng số hạt mang điện của X là 12. Các nguyên tố X và Y là :
- A Mg và Ca
- B Si và O
- C Al và Cl
- D Na và S
Đáp án: B
Phương pháp giải:
Viết cấu hình e của nguyên tử nguyên tố X dựa vào dữ kiện tổng số e phân lớp p là 8
=> nguyên tử nguyên tố X
=> nguyên tử nguyên tố Y
Lời giải chi tiết:
Cấu hình e của X: 1s22s22p63s23p2
ZX = 14 => X là Si => số hạt mang điện trong X là 28
=> Số hạt mang điện trong Y là 16 => ZY = 8
=> Y là Oxi
Đáp án B
Câu hỏi 10 :
Nguyên tố X thuộc loại nguyên tố d, nguyên tử của X có 5 electron hoá trị và lớp electron ngoài cùng thuộc lớp 4. Cấu hình electron của X là:
- A 1s2 2s2 2p6 3s2 3p6 3d3 4s2
- B 1s2 2s2 2p6 3s2 3p6 4s2 3d3
- C 1s2 2s2 2p6 3s2 3p6 3d5 4s2
- D 1s22s2 2p2 3s3 3p 3d10 4s2 4p3 .
Đáp án: A
Lời giải chi tiết:
Đáp án A
Câu hỏi 11 :
A và B là hai nguyên tố trong cùng một nhóm và ở hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số hạt proton trong hạt nhân của A và B là 32. Hai nguyên tố đó là:
- A Mg và Ca
- B O và S
- C N và Si
- D C và Si
Đáp án: A
Phương pháp giải:
Hai nguyên tố ở chu kì kế tiếp nhau trong bảng tuần hoàn có số hiệu nguyên tử hơn kém nhau 8 hoặc 18. HS xét từng trường hợp để tìm số hiệu nguyên tử
Lời giải chi tiết:
Do A,B thuộc cùng 1 nhóm và ở 2 chu kì liên tiếp
=> ZA – ZB = 2 hoặc 8 hoặc 18 hoặc 32
=> Do ZA + ZB = 32
Mà ZA – ZB = 8
=> ZA = 20 ; ZB = 12=> A là Mg và B là Ca
Đáp án A
Câu hỏi 12 :
Hòa tan hoàn toàn 7,30 gam hỗn hợp hai kim loại kiềm X, Y (MX < MY) thuộc hai chu kì liên tiếp vào 200 gam nước thu được dung dịch Z và 7,84 lít khí hidro (đktc). Nồng độ phần trăm của YOH trong dung dịch Z là
- A 2,904%.
- B 6,389%.
- C 2,894%.
- D 1,670%.
Đáp án: A
Phương pháp giải:
Viết PTHH và tính toán theo PTHH.
Lời giải chi tiết:
Gọi công thức chung của 2 kim loại là M
M + H2O → MOH + 0,5 H2
0,7 ← 0,35 (mol)
M = 7,3/0,7 = 10,43 => Li và Na
Đặt nLi = x; nNa = y (mol)
\(\left\{ \begin{gathered}
7x + 23y = 7,3 \hfill \\
x + y = 0,7 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x = 0,55 \hfill \\
y = 0,15 \hfill \\
\end{gathered} \right.\)
mdd sau phản ứng = mKL + mH2O – mH2 = 7,3 + 200 – 0,35.2 = 206,6 (g)
\( \to C{\% _{NaOH}} = \frac{{0,15.40}}{{206,6}}.100\% = 2,904\% \)
Đáp án A
Câu hỏi 13 :
Nguyên tố Y là phi kim thuộc chu kì 2 của BTH, Y tạo được hợp chất khí với hiđro và công thức oxit cao nhất là YO2. Hợp chất tạo bởi Y và kim loại M là MY2 trong đó Y chiếm 37,5% về khối lượng. M là
- A Mg.
- B Cu.
- C Al.
- D Ca.
Đáp án: D
Phương pháp giải:
*Xác định Y:
Y thuộc chu kì 2 => số lớp e
Công thức oxit cao nhất của Y là YO2 => hóa trị của Y => nhóm => số e lớp ngoài cùng
=> Cấu hình e của Y và xác định Y
*Xác định M: Từ % khối lượng Y trong hợp chất MY2 ta xác định được khối lượng mol của M => M
Lời giải chi tiết:
*Xác định Y:
Y thuộc chu kì 2 => Y có 2 lớp e
Công thức oxit cao nhất của Y là YO2 => Y có hóa trị IV => Y thuộc nhóm IVA => Y có 4e lớp ngoài cùng
=> Cấu hình e của Y: 1s22s22p2 => Y là Cacbon
*Xác định M: Hợp chất MC2: \(\% {m_C} = \frac{{2.12}}{{M + 2.12}}.100\% = 37,5\% \to M = 40(Ca)\)
Vậy M là Ca
Đáp án D
Câu hỏi 14 :
Hai nguyên tố X, Y ở cùng nhóm A và thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số proton của 2 nguyên tử thuộc hai nguyên tố là 44 (ZX <ZY). Vị trí của X trong bảng tuần hoàn là:
- A chu kì 3, nhóm IIA
- B chu kì 3, nhóm IIIA
- C chu kì 4, nhóm IIA
- D chu kì 4, nhóm IIIA
Đáp án: B
Phương pháp giải:
Hai nguyên tố X, Y ở cùng nhóm A và thuộc cùng hai chu kì liên tiếp trong bảng tuần hoàn.
→ ZY= ZX + 8 hoặc ZY= ZX + 18
Xét 2 trường hợp trên để tìm ZX và ZY.
Từ đó xác định được vị trí của X trong bảng tuần hoàn.
Lời giải chi tiết:
Hai nguyên tố X, Y ở cùng nhóm A và thuộc cùng hai chu kì liên tiếp trong bảng tuần hoàn.
→ ZY= ZX + 8 hoặc ZY= ZX + 18
*TH1: Xét ZY= ZX + 8
Theo đề bài tổng số proton của 2 nguyên tử là 44 nên ZX + ZY = 44
Giải hệ ta có: ZX= 18 và ZY= 26
Cấu hình electron nguyên tử của Y là 1s22s22p63s23p63d64s2. Vậy Y thuộc nhóm VIB.
Vậy trường hợp này loại vì theo đề bài X, Y ở cùng nhóm A.
*TH2: Xét ZY= ZX + 18
Theo đề bài tổng số proton của 2 nguyên tử là 44 nên ZX + ZY = 44
Giải hệ ta có: ZX= 13, ZY= 31
Cấu hình electron của X là 1s22s22p63s23p1, vậy X thuộc chu kì 3, nhóm IIIA
Cấu hình electron của Y là 1s22s22p63s23p63d104s23p1, vậy Y thuộc chu kì 4, nhóm IIIA
Đáp án B
Câu hỏi 15 :
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì có tổng số điện tích hạt nhân là 29, biết ZX < ZY. Y thuộc chu kì và nhóm nào sau đây?
- A chu kì 3, nhóm IVA
- B chu kì 3, nhóm VA
- C chu kì 2, nhóm IVA
- D chu kì 3, nhóm IIIA
Đáp án: B
Phương pháp giải:
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì nên ZY – ZX = 1
Từ đề bài lập hệ phương trình tìm ZX và ZY. Từ đó xác định vị trí của X và Y trong bảng tuần hoàn.
Lời giải chi tiết:
Giả sử: ZY > ZX, có: ZX + ZY = 29 (1)
Vì X, Y đứng kế tiếp nhau trong một chu kì nên ZY – ZX = 1 (2)
Giải hệ gồm (1) và (2) ta được: ZX = 14; ZY = 15
ZX = 14: 1s22s22p63s23p2 → chu kì 3, nhóm IVA
ZY = 15: 1s22s22p63s23p3 → chu kì 3, nhóm VA
Đáp án B
Câu hỏi 16 :
Hai nguyên tử của nguyên tố X và Y có cấu hình electron ở lớp ngoài cùng là 4pa và 4sb. Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7. Biết X không phải là khí hiếm. Vậy Y và X lần lượt là:
- A K và Br
- B Ca và Br
- C K và S
- D Ca và S
Đáp án: B
Phương pháp giải:
Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7 nên a + b= 7 với 1≤b≤6 và b = 1 hoặc b = 2
*TH1: Nếu b= 1 thì a = 6.
*TH2: Nếu b= 2 thì a = 5.
Xét 2 trường hợp trên để tìm X và Y phù hợp.
Lời giải chi tiết:
Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7 nên a + b= 7 với 1 ≤ a ≤ 6 và b = 1 hoặc b = 2
*TH1: Nếu b= 1 thì a = 6.
Cấu hình electron của X là 1s22s22p63s23p63d104s24p6. X có 8 electron ở lớp ngoài cùng nên X là khí hiếm.
Vậy trường hợp này loại.
*TH2: Nếu b= 2 thì a = 5.
Cấu hình electron của X là 1s22s22p63s23p63d104s24p5. Vậy X là nguyên tố Br.
Cấu hình electron của Y là 1s22s22p63s23p64s2. Vậy Y là nguyên tố Ca.
Đáp án B
Câu hỏi 17 :
Hai nguyên tố X và Y thuộc hai nhóm A kế tiếp nhau trong một chu kì có tổng số proton trong hai hạt nhân nguyên tử là 51. Số hiệu nguyên tử của X và Y lần lượt là:
- A 25 và 26
- B 20 và 31
- C 21 và 30
- D 16 và 35
Đáp án: B
Phương pháp giải:
Giả sử: ZY > ZX, có: ZX + ZY = 51 (1)
Vì X, Y đứng kế tiếp nhau trong một chu kì nên có 2 trường hợp:
TH1: ZY – ZX = 1 (2)
TH2: ZY – ZX = 11 (3)
Xét 2 trường hợp trên để xác định trường hợp thỏa mãn.
Lời giải chi tiết:
Giả sử: ZY > ZX, có: ZX + ZY = 51 (1)
Vì X, Y đứng kế tiếp nhau trong một chu kì nên có 2 trường hợp:
TH1: ZY – ZX = 1 (2)
Giải hệ gồm (1) và (2) ta được: ZX = 25; ZY = 26
ZX = 25: 1s22s22p63s23p63d54s2→ chu kì 4, nhóm VII B
ZY = 26: 1s22s22p63s23p63d64s2 → chu kì 4, nhóm VIIIB
Trường hợp này loại vì 2 nguyên tố X, Y thuộc nhóm B , còn đề bài cho 2 nguyên tố X và Y thuộc nhóm A.
TH2:
ZY – ZX = 11 (3)
Giải hệ gồm (1) và (3) ta được: ZX = 20; ZY = 31
ZX = 20: 1s22s22p63s23p64s2→ chu kì 4, nhóm IIA
ZY = 31: 1s22s22p63s23p63d104s24p1 → chu kì 4, nhóm IIIA
Trường hợp 2 cả 2 nguyên tố X và Y thuộc nhóm A nên thỏa mãn.
Số hiệu nguyên tử của X và Y lần lượt là 20 và 31.
Đáp án B
Câu hỏi 18 :
Vị trí các nguyên tố X, Y, R, T trong bảng tuần hoàn như sau:
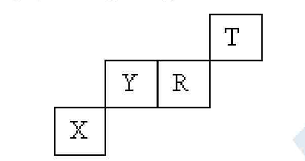
X có cấu hình electron lớp ngoài cùng là 4s24p2. Tổng số proton của 3 nguyên tử X, R, T là:
- A 56
- B 57
- C 40
- D 64
Đáp án: B
Phương pháp giải:
Dựa vào vị trí của X, Y, R, T để tìm cấu hình electron của các nguyên tử. Từ đó xác định được tổng số proton của 3 nguyên tử X, R, T.
Lời giải chi tiết:
Vì X có cấu hình electron lớp ngoài cùng là 4s24p2 nên cấu hình electron đầy đủ của X là 1s22s22p63s23p63d104s24p2. Vậy nguyên tử X có 32 electron, 32 proton. Nguyên tố X thuộc nhóm IVA.
Gọi nguyên tố Z là nguyên tố cùng nhóm với X và đứng ngay trước nguyên tố Y.
Vì X và Z thuộc cùng nhóm và nằm ở 2 chu kì liên tiếp nên xét các trường hợp:
TH1: nguyên tố Z có 32- 8= 24 electron.
Cấu hình electron nguyên tử của Z là 1s22s22p63s23p63d54s1. Nguyên tố Z thuộc nhóm VIB.
Vậy trường hợp này loại.
TH2: nguyên tố Z có 32- 18 = 14 electron.
Cấu hình electron nguyên tử của Z là 1s22s22p63s23p2. Nguyên tố Z thuộc nhóm IVA.
Vậy trường hợp 2 thỏa mãn.
Nguyên tố Z đứng ngay trước nguyên tố Y nên Y có số hiệu nguyên tử là 14 + 1= 15
Suy ra số proton của nguyên tử Y bằng 15.
Nguyên tố Y đứng ngay trước nguyên tố R nên R có số hiệu nguyên tử là 15 + 1= 16
Suy ra số proton của nguyên tử R bằng 16.
Gọi Q là nguyên tố thuộc cùng nhóm với nguyên tố R và đứng trước nguyên tố T
Suy ra số hiệu nguyên tử Q bằng 16 – 8= 8 và số hiệu nguyên tử nguyên tố T là 8 + 1= 9
Tổng số proton của 3 nguyên tử X, R, T là: 32 + 16 + 9= 57
Đáp án B
Câu hỏi 19 :
X và Y là 2 nguyên tố nằm trong 2 nhóm A kế tiếp nhau trong bảng tuần hoàn dạng ngắn. X thuộc nhóm VIIA. Tổng số hạt proton trong 2 hạt nhân của X và Y là 25 (biết ZX < ZY). Biết X tác dụng được với Y. Các nguyên tố X, Y tương ứng là:
- A Ne và P
- B O và Cl
- C F và S
- D N và Ar
Đáp án: C
Phương pháp giải:
Vì X thuộc nhóm VIIA nên Y thuộc nhóm VIA
Ta có: PX + PY= 25
Từ đó xác định được số hiệu nguyên tử của X và Y và xác định được tên của X và Y.
Lời giải chi tiết:
Vì X thuộc nhóm VIIA nên Y thuộc nhóm VIA
Ta có: PX + PY= 25 → X là F (Z= 9) và Y là S (Z=16) hoặc X là Cl (Z=17) và Y là O (Z=8)
Vì X tác dụng được với Y nên X là F và Y là S.
Đáp án C
Câu hỏi 20 :
Nguyên tử của hai nguyên tố X và Y có tổng số electron lớp ngoài cùng bằng 12. Ở trạng thái cơ bản, số electron p của X nhiều hơn của Y là 8. Biết nguyên tử của nguyên tố X có 3 lớp electron và Y có số lớp electron ít hơn X. Phát biểu nào sau đây đúng?
- A X thuộc nhóm VA; Y thuộc nhóm IIIA
- B X thuộc nhóm VIIA, Y thuộc nhóm VA
- C X thuộc nhóm VIA, Y thuộc nhóm IIIA
- D X thuộc nhóm IVA, Y thuộc nhóm VA
Đáp án: B
Phương pháp giải:
Vì tổng số electron lớp ngoài cùng của X và Y bằng 12
→ 2 + 8 < số electron ở lớp ngoài cùng = 12 < 8.2=16 nên X và Y đều có electron lớp ngoài cùng đang điền trên phân lớp p. Suy ra cấu hình electron của X, Y là:
X: 1s22s22p63s23pa
Y: 1s22s22pb
Từ đề bài xác định các giá trị a và b. Từ đó tìm được phát biểu đúng.
Lời giải chi tiết:
Vì tổng số electron lớp ngoài cùng của X và Y bằng 12
→ 2 + 8 < số electron ở lớp ngoài cùng = 12 < 8.2=16 nên X và Y đều có electron lớp ngoài cùng đang điền trên phân lớp p. Suy ra cấu hình electron của X, Y là:
X: 1s22s22p63s23pa
Y: 1s22s22pb
Suy ra (2+a) + (2+b)= 12 và 6 + a = b+8
Giải hệ trên ta có a = 5 và b = 3
Vậy X thuộc nhóm VIIA và Y thuộc nhóm VA
Đáp án B
